
 在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )
在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )| A. | 在t℃时,AgCL的Ksp为4×10-10 | |
| B. | 在t℃时,c点溶液中一定有AgCl沉淀析出 | |
| C. | 在t℃时,AgCl的溶解度约为2.9×10-4g | |
| D. | d点溶液,温度升高后c(Ag+)、c(Cl-)均不变 |
分析 A.根据图中b点的c(Ag+)和c(Cl-)可得该温度下AgCl的Ksp;
B.c点时c(Ag+)•c(Cl-)>Ksp;
C.根据Ksp计算100mL溶液中的AgCl的浓度、质量,可计算溶解度;
D.升高温度促进AgCl的溶解.
解答 解:A.图中b点的c(Ag+)=c(Cl-)=2×10-5mol/L,则该温度下AgCl的Ksp=(Ag+)•c(Cl-)=4×10-10,故A正确;
B.c点时c(Ag+)大于d,而c(Cl-)相等,则c(Ag+)•c(Cl-)>Ksp,一定有AgCl沉淀析出,故B正确;
C.在t℃时,AgCl饱和溶液中c(Ag+)=c(Cl-)=2×10-5mol/L,则100mL溶液中n(AgCl)=2×10-5mol/L×0.1L=2×10-6mol,m(AgCl)=2×10-6mol×143.5g/mol=2.9×10-4g,AgCl饱和溶液的密度与水的密度近似相等,则可知在t℃时,AgCl的溶解度约为2.9×10-4g,故C正确;
D.升高温度,促进溶解,AgCl的溶解度增大,c(Ag+)、c(Cl-)均会增大,故D错误.
故选D.
点评 本题考查了沉淀溶解平衡曲线,难度中等,曲线上的每个点都为AgCl饱和溶液,曲线以下为不饱和溶液,注意掌握Ksp的表达式及简单计算方法.


科目:高中化学 来源: 题型:选择题
| A. | 各能层含有电子数为2n2 | |
| B. | 各能层的能级都是从s能级开始至f能级结束 | |
| C. | 各能层含有的能级数为n-l | |
| D. | 各能级的原子轨道数按s、p、d、f的顺序依次为1、3、5、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
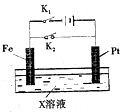 如图是一个电化学过程的示意图,请回答下列问题:
如图是一个电化学过程的示意图,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
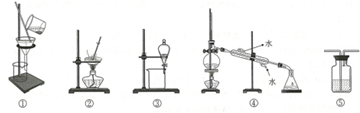
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应体系中Au2O是氧化剂 | |
| B. | Na2S4O6是还原产物 | |
| C. | 该反应体系中起还原作用的元素是Au2O中+1价的Au | |
| D. | 该反应体系中每转移2mol电子则消耗1molH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
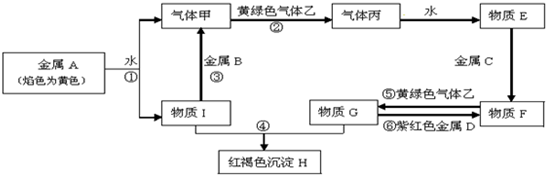
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2 | B. | NaOH | C. | Ba(NO3)2 | D. | Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.7g | B. | 8.1g | C. | 5.4g | D. | 10.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com