
【题目】25℃时,0.1mol/L的HA溶液中 ![]() =1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
=1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
(1)HA是________(填“强电解质”或“弱电解质”,下同),BOH是________。
(2)HA的电离方程式是________。其中由水电离出的c(H+)=________mol/L。
(3)在加水稀释HA的过程中,随着水量的增加而减小的是_______(填字母)。
A.![]() B.
B.![]() C.c(H+)与c(OH﹣)的乘积D.c(OH﹣)
C.c(H+)与c(OH﹣)的乘积D.c(OH﹣)
(4)将等体积等物质的量浓度的HA溶液和BOH溶液混合后的溶液呈________性,请用离子方程式解释其原因_______________________,混合溶液中各离子浓度由大到小的顺序是_______________________。
(5)常温下pH=12的BOH溶液100mL,加0.01mol/L NaHSO4使溶液的pH为11。(混合溶液体积变化忽略不计),应加 NaHSO4________mL。(保留到小数点后一位)
【答案】 弱电解质 强电解质 HAH++A﹣ 10﹣12 B 碱 A﹣+H2OHA+OH﹣ c(B+)>c(A﹣) >c(OH﹣) >c(H+) 81.8
【解析】(1) 25℃时,0.1mol/L的HA溶液中 ![]() =1010,c(H+)=0.01mol/L,HA是弱电解质;0.01mol/L的BOH溶液pH=12,则c(OH﹣)=0.01mol/L,BOH是强电解质。(2)HA是弱电解质,其电离方程式是HAH++A﹣;由水电离出的c(H+)水= c(OH﹣)水=10﹣12 mol/L。(3)在加水稀释HA的过程中,A.
=1010,c(H+)=0.01mol/L,HA是弱电解质;0.01mol/L的BOH溶液pH=12,则c(OH﹣)=0.01mol/L,BOH是强电解质。(2)HA是弱电解质,其电离方程式是HAH++A﹣;由水电离出的c(H+)水= c(OH﹣)水=10﹣12 mol/L。(3)在加水稀释HA的过程中,A.![]() 增大, B.
增大, B.![]() 减小,C.c(H+)与c(OH﹣)的乘积不变,D.氢离子浓度减小,c(OH﹣)增大;随着水量的增加而减小的是B。(4)将等体积等物质的量浓度的HA溶液和BOH溶液混合生成强碱弱酸盐,该盐溶液呈碱性,原因是:A﹣+H2OHA+OH﹣,混合溶液中各离子浓度由大到小的顺序是:c(B+)>c(A﹣) >c(OH﹣) >c(H+)。(5)(0.01mol/L×0.1L—0.01mol/L×VL)/(0.1L+ VL)==0.001mol/L,V=0.0818L,即应加 NaHSO4体积为81.8mL。
减小,C.c(H+)与c(OH﹣)的乘积不变,D.氢离子浓度减小,c(OH﹣)增大;随着水量的增加而减小的是B。(4)将等体积等物质的量浓度的HA溶液和BOH溶液混合生成强碱弱酸盐,该盐溶液呈碱性,原因是:A﹣+H2OHA+OH﹣,混合溶液中各离子浓度由大到小的顺序是:c(B+)>c(A﹣) >c(OH﹣) >c(H+)。(5)(0.01mol/L×0.1L—0.01mol/L×VL)/(0.1L+ VL)==0.001mol/L,V=0.0818L,即应加 NaHSO4体积为81.8mL。


科目:高中化学 来源: 题型:
【题目】I是一种重要的有机化合物,其合成路线如图所示:
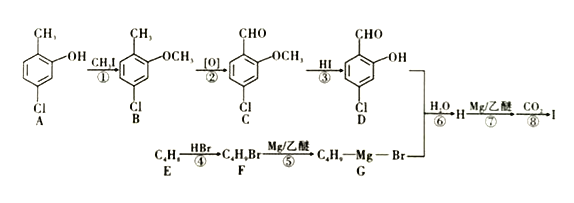
已知:
①有机物F结构中只有一种等效氢;
②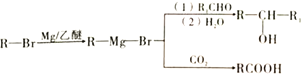
试根据相关知识回答下列问题:
(1)烃E的名称为_________,物质B含有的官能团的名称为________,B到C的反应类型是_________。
(2)在该过程中步骤①③两步设计的目的是_______________________,如果要检验合成的化合物B中是否含有A时,可用_______试剂。
(3)C能与新制的Cu(OH)2反应生成砖红色沉淀,试写出该反应的化学方程式:_____________________,化合物I的结构简式为_____________________________。
(4)芳香族化合物M(C8H7O2Br)能发生银镜反应,且苯环上只有两个取代基,满足上述条件的同分异构体一共有_______种。(提示:含有“-O-Br”结构的物质不稳定,不考虑)
(5)参照上述合成路线,以乙醇为基本原料(其他试剂自选),设计制备CH3CH2COOCH2CH3的合成路线。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.氯化钠固体不导电,所以氯化钠不是电解质
C.氯化氢溶液能导电,所以氯化氢是电解质
D.氯气溶于水能导电,所以氯气是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时纯水的电离度为a1,pH=2的醋酸溶液的电离度为a2,pH=12的氢氧化钠溶液中水的电离度为a3。若将上述醋酸与氢氧化钠溶液等体积混合,所得溶液中水的电离度为a4。下列关系式中正确的是
A. a3=a2<a1<a4 B. a2=a3<a4<a1
C. a2<a3<a1<a4 D. a1<a2<a3<a4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数。
(1)写出A的元素符号___________________;元素C的一种原子(中子数为14)的原子符号_______________;
(2)B的阴离子结构示意图________;A、B组成的化合物的化学式__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的氧气和臭氧(O3),它们的物质的量之比为__________,所含分子数之比为__________,所含原子数之比为__________。
(2)中和含0.2molHCl的稀盐酸,需NaOH固体的质量为__________g。
(3)某气态氧化物的化学式为RO2,标准状况下1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_____,R的相对原子质量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁烷与异丁烷互为同分异构体的依据是
A. 具有相同的化学性质 B. 具有相同的物理性质
C. 具有相同的相对分子质量 D. 分子式相同,分子结构不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质,都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
①C2H5OH②CH3COOH(aq)③H2O
A.①>②>③B.②>①>③C.③>①>②D.②>③>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com