
 ������������Ծ�ϵ�д�
������������Ծ�ϵ�д� �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д� ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȩ��һ����Ҫ�Ļ�����Ʒ���������ü״������Ʊ�����Ӧʽ���£�
��CH30H(g)=CH20(g)+H2(g) ��H1=+84.2kJ��mol-1
��Ӧ��ϵ��ͨ��������ͨ����Ӧ��2H2(g)+O2(g)=2H2O(g) ��H2=-483.6 kJ��mol-1 �ṩ��Ӧ������������Ҫʹ��Ӧ�¶�ά����700��c��������м״������������ʵ���֮��Ϊ
A.5.74��1 B.11.48��1 C.1��l D.2��l
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣���ȩ��һ����Ҫ�Ļ�����Ʒ�������ü״��������Ʊ���̬��ȩ����ȩ����̬�״�ת����������ϵ��ͼ��ʾ��
��1���״�������ת��Ϊ��ȩ�ķ�Ӧ����������������ȡ����ȡ�����Ӧ.
��2�����̢�����̢�ķ�Ӧ���Ƿ���ͬ������������������ ��
��3���ϳɼ״�����Ҫ��ӦΪ��CO(g)+2H2(g)CH3OH(g) ��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
| T/�� | T1 | T2 | T3 |
| K | 1/1000 | 1/40 | 25 |
T1��T2��T3�Ĵ�С��ϵΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��㶫ʡ������ѧ�߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ������
��8�֣���ȩ��һ����Ҫ�Ļ�����Ʒ�������ü״��������Ʊ���̬��ȩ����ȩ����̬�״�ת����������ϵ��ͼ��ʾ��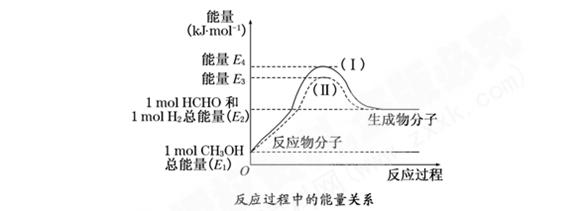
��1���״�������ת��Ϊ��ȩ�ķ�Ӧ����������������ȡ����ȡ�����Ӧ.
��2�����̢�����̢�ķ�Ӧ���Ƿ���ͬ������������������  ��
��
��3���ϳɼ״�����Ҫ��ӦΪ��CO(g)+2H2(g) CH3OH(g)��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
CH3OH(g)��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
| T/�� | T1 | T2 | T3 |
| K | 1/1000 | 1/40 | 25 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�갲��ʡ���������꼶��һ�ν�ѧ������鿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȩ��һ����Ҫ�Ļ�����Ʒ���������ü״������Ʊ�����Ӧʽ���£�
��CH30H(g)=CH20(g)+H2(g) ��H1=+84.2kJ��mol-1
��Ӧ��ϵ��ͨ��������ͨ����Ӧ��2H2(g)+O2(g)=2H2O(g) ��H2=-483.6 kJ��mol-1 �ṩ��Ӧ������������Ҫʹ��Ӧ�¶�ά����700��c��������м״������������ʵ���֮��Ϊ
A.5.74��1 B.11.48��1 C.1��l D.2��l
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��㶫ʡ�߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ������
��8�֣���ȩ��һ����Ҫ�Ļ�����Ʒ�������ü״��������Ʊ���̬��ȩ����ȩ����̬�״�ת����������ϵ��ͼ��ʾ��
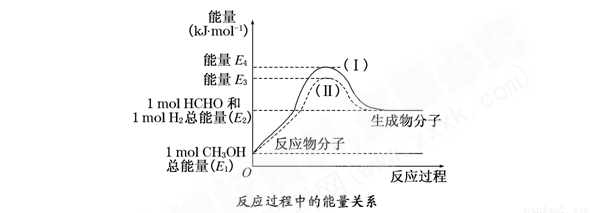
��1���״�������ת��Ϊ��ȩ�ķ�Ӧ����������������ȡ����ȡ�����Ӧ.
��2�����̢�����̢�ķ�Ӧ���Ƿ���ͬ������������������ ��
��3���ϳɼ״�����Ҫ��ӦΪ��CO(g)+2H2(g) CH3OH(g) ��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
CH3OH(g) ��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
|
T/�� |
T1 |
T2 |
T3 |
|
K |
1/1000 |
1/40 |
25 |
T1��T2��T3�Ĵ�С��ϵΪ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com