
 µē³ŲµÄ”°ĄķĀŪ±ČÄÜĮæ”±Öøµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻĄķĀŪÉĻÄÜŹĶ·ÅµÄ×ī“óµēÄÜ£®”°½šŹō£ØM£©〜æÕĘųµē³Ų”±£ØČēĻĀĶ¼£©¾ßÓŠŌĮĻŅ׵Ɣ¢ÄÜĮæĆܶČøßµČÓÅµć£®øĆĄąµē³Ų·ÅµēµÄ×Ü·“Ó¦·½³ĢŹ½ĪŖ£ŗ4M+nO2+2nH2OØT4M£ØOH£© n£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
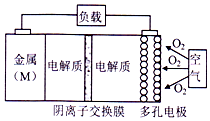
µē³ŲµÄ”°ĄķĀŪ±ČÄÜĮæ”±Öøµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻĄķĀŪÉĻÄÜŹĶ·ÅµÄ×ī“óµēÄÜ£®”°½šŹō£ØM£©〜æÕĘųµē³Ų”±£ØČēĻĀĶ¼£©¾ßÓŠŌĮĻŅ׵Ɣ¢ÄÜĮæĆܶČøßµČÓÅµć£®øĆĄąµē³Ų·ÅµēµÄ×Ü·“Ó¦·½³ĢŹ½ĪŖ£ŗ4M+nO2+2nH2OØT4M£ØOH£© n£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ”°½šŹō£ØM£©〜æÕĘųµē³Ų”±·Åµē¹ż³ĢµÄÕż¼«·“Ó¦Ź½£ŗO2+2H2O+4e-=4M£ØOH£©n | |
| B£® | ±Č½ĻMg”¢Al”¢ZnČżÖÖ”°½šŹō-æÕĘųµē³Ų”±£¬”°Al-æÕĘųµē³Ų”±µÄĄķĀŪ±ČÄÜĮæ×īøß | |
| C£® | µē½āÖŹČÜŅŗÖŠµÄŅõĄė×Ó“Óøŗ¼«ĒųŅĘĻņÕż¼«Ēų | |
| D£® | ŌŚ”°M-æÕĘųµē³Ų”±ÖŠ£¬ĪŖ·ĄÖ¹øŗ¼«Ēų³Į»żMg£ØOH£©2£¬ŅĖ²ÉÓĆÖŠŠŌµē½āÖŹ¼°ŃōĄė×Ó½»»»Ä¤ |
·ÖĪö A£®Õż¼«ÉĻŃõµē½āÖŹČÜŅŗÖŠµÄŅõĄė×Ó“Óøŗ¼«ĒųŅĘĻņÕż¼«ĒųĘųµĆµē×ÓŗĶĖ®·“Ӧɜ³ÉOH-£»
B£®µē³ŲµÄ”°ĄķĀŪ±ČÄÜĮæ”±Öøµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻĄķĀŪÉĻÄÜŹĶ·Å³öµÄ×ī“óµēÄÜ£¬Ōņµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻŹ§Č„µē×ÓµÄĪļÖŹµÄĮæŌ½¶ąŌņµĆµ½µÄµēÄÜŌ½¶ą£»
C£®µē½āÖŹČÜŅŗÖŠµÄŅõĄė×Ó“ÓÕż¼«ĒųŅĘĻņøŗ¼«Ēų£»
D£®øŗ¼«ÉĻMgŹ§µē×ÓÉś³ÉMg2+£¬ĪŖ·ĄÖ¹øŗ¼«Ēų³Į»żMg£ØOH£©2£¬ŌņŅõ¼«ĒųČÜŅŗ²»ÄÜŗ¬ÓŠ“óĮæOH-£®
½ā“š ½ā£ŗA£®Õż¼«ÉĻŃõĘųµĆµē×ÓŗĶĖ®·“Ӧɜ³ÉOH-£¬ŅņĪŖŹĒŅõĄė×Ó½»»»Ä¤£¬ĖłŅŌŃōĄė×Ó²»ÄܽųČėÕż¼«ĒųÓņ£¬ŌņÕż¼«·“Ó¦Ź½ĪŖO2+2H2O+4e-=4OH-£¬¹ŹAÕżČ·£»
B£®µē³ŲµÄ”°ĄķĀŪ±ČÄÜĮæ”±Öøµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻĄķĀŪÉĻÄÜŹĶ·Å³öµÄ×ī“óµēÄÜ£¬Ōņµ„Ī»ÖŹĮæµÄµē¼«²ÄĮĻŹ§Č„µē×ÓµÄĪļÖŹµÄĮæŌ½¶ąŌņµĆµ½µÄµēÄÜŌ½¶ą£¬¼ŁÉčÖŹĮ涼ŹĒ1gŹ±£¬ÕāČżÖÖ½šŹō×ŖŅʵē×ÓĪļÖŹµÄĮæ·Ö±šĪŖ$\frac{1g}{24g/mol}$=$\frac{1}{12}$mol”¢$\frac{1g}{27g/mol}$”Į3=$\frac{1}{9}$mol”¢$\frac{1g}{65g/mol}$=$\frac{1}{32.5}$mol£¬ĖłŅŌAl-æÕĘųµē³ŲµÄĄķĀŪ±ČÄÜĮæ×īøߣ¬¹ŹBÕżČ·£»
C£®µē½āÖŹČÜŅŗÖŠµÄŅõĄė×Ó“ÓÕż¼«ĒųŅĘĻņøŗ¼«Ēų£¬¶ų²»ŹĒ“Óøŗ¼«ĒųŅĘĻņÕż¼«Ēų£¬¹ŹC“ķĪó£»
D£®øŗ¼«ÉĻMgŹ§µē×ÓÉś³ÉMg2+£¬ĪŖ·ĄÖ¹øŗ¼«Ēų³Į»żMg£ØOH£©2£¬ŌņŅõ¼«ĒųČÜŅŗ²»ÄÜŗ¬ÓŠ“óĮæOH-£¬ĖłŅŌŅĖ²ÉÓĆÖŠŠŌµē½āÖŹ¼°ŃōĄė×Ó½»»»Ä¤£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌµē³ŲŌĄķ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪöÅŠ¶Ļ”¢»ńČ”ŠÅĻ¢½ā“šĪŹĢā¼°¼ĘĖćÄÜĮ¦£¬Ć÷Č·ø÷øöµē¼«ÉĻ·¢ÉśµÄ·“Ó¦”¢Ąė×Ó½»»»Ä¤×÷ÓĆ”¢·“Ó¦ĖŁĀŹÓ°ĻģŅņĖŲ”¢Ńõ»Æ»¹Ō·“Ó¦¼ĘĖćŹĒ½ā±¾Ģā¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ”ś
”ś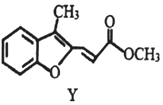 ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
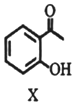
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ĪļÖŹXµÄ·Ö×ÓŹ½ĪŖC8H8O2 | |
| B£® | ĪļÖŹXÖŠĖłÓŠĢ¼Ō×ÓæÉÄÜŌŚĶ¬Ņ»Ę½ĆęÄŚ | |
| C£® | ĪļÖŹYµÄ1HŗĖ“Ź²ÕńĘ×Ķ¼ÖŠÓŠ8×éĢŲÕ÷·å | |
| D£® | 1molY×ī¶ąæÉÓė6molĒāĘų·¢Éś¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬11.2LH2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA | |
| B£® | 7.8g¹żŃõ»ÆÄĘÓė×ćĮæĖ®·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.2NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬6gO2ŗĶ26gO3»ģŗĻĘųĢåÖŠµÄŌ×Ó×ÜŹżĪŖ2NA | |
| D£® | 100mL0.1mol/LµÄNa2SO4ČÜŅŗÖŠ£¬Ėłŗ¬Ąė×Ó×ÜŹżĪŖ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬Q3Y2ÓėĖ®æɾēĮŅ·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖMg3N2+6H2O=3Mg£ØOH£©2+2NH3”ü
£¬Q3Y2ÓėĖ®æɾēĮŅ·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖMg3N2+6H2O=3Mg£ØOH£©2+2NH3”ü²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | v£ØSiF4£©ĻūŗÄ=4v£ØHF£©Éś³É | B£® | HF µÄĢå»ż·ÖŹż²»ŌŁ±ä»Æ | ||
| C£® | ČŻĘ÷ÄŚĘųĢåŃ¹Ēæ²»ŌŁ±ä»Æ | D£® | ČŻĘ÷ÄŚĘųĢå×ÜÖŹĮæ²»ŌŁ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuCl2ČÜŅŗÓė Fe µÄ·“Ó¦£ŗCu2++FeØTCu+Fe3+ | |
| B£® | ĀČĘųÓėĖ®·“Ó¦£ŗCl2+H2O?H++Cl-+HClO | |
| C£® | ĒāŃõ»ÆĀĮČÜŅŗÓėŃĪĖįµÄ·“Ó¦£ŗOH-+H+=H2O | |
| D£® | Ė®¹øÖŠµÄCaCO3ÓĆCH3COOHČÜŅŗ³żČ„£ŗCaCO3+2H+ØTCa2++H2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | “ļĘ½ŗāŹ±£¬6v£ØH2£©Õż=2 v£ØCO2£©Äę | B£® | Õż·“Ó¦µÄ·“Ó¦ČČ£ŗ”÷H£¼0 | ||
| C£® | Ę½ŗā³£Źż£ŗKb£¼Kc | D£® | ĒśĻßIµÄĶ¶ĮĻ£ŗn£ØH2£©£ŗn£ØCO2£©=2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 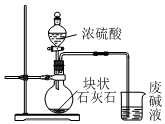 ÓĆ×°ÖĆ¼×ÖĘČ”CO2²¢ĶØČė·Ļ¼īŅŗ | |
| B£® |  ÓĆ×°ÖĆŅŅ“ÓĻĀæŚ·Å³ö·ÖŅŗŗóÉĻ²ćµÄÓŠ»śĻą | |
| C£® | 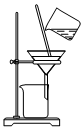 ÓĆ×°ÖƱū·ÖĄėĖ®ĻąÖŠ¼ÓČėCa£ØOH£©2²śÉśµÄCaCO3 | |
| D£® |  ÓĆ×°Öƶ”½«ĀĖŅŗÕō·¢½į¾§µĆµ½NaOH¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
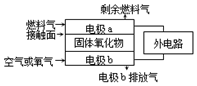 ¹ĢĢåŃõ»ÆĪļČ¼ĮĻµē³Ų£ØSOFC£©ŅŌ¹ĢĢåŃõ»ÆĪļ×÷ĪŖµē½āÖŹ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠ¹ŲÓŚ¹ĢĢåČ¼ĮĻµē³ŲµÄÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
¹ĢĢåŃõ»ÆĪļČ¼ĮĻµē³Ų£ØSOFC£©ŅŌ¹ĢĢåŃõ»ÆĪļ×÷ĪŖµē½āÖŹ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠ¹ŲÓŚ¹ĢĢåČ¼ĮĻµē³ŲµÄÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ¹ĢĢåŃõ»ÆĪļµÄ×÷ÓĆŹĒČƵē×ÓŌŚµē³ŲÄŚĶعż | |
| B£® | ¹ĢĢåŃõ»ÆĪļÖŠO2-“Óa¼«Ļņb¼«ŅĘ¶Æ | |
| C£® | µē¼«bĪŖµē³ŲµÄøŗ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗO2+4e-=2O2- | |
| D£® | ČōŅŌC3H8ĪŖČ¼ĮĻĘų£¬Ōņ½Ó“„ĆęÉĻ·¢ÉśµÄ·“Ó¦ĪŖC3H8-20e-+10O2-ØT3CO2+4H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com