
某有机物的结构为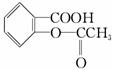 ,在一定条件下此有机物可能发生的反应有
,在一定条件下此有机物可能发生的反应有
( )
①中和反应 ②银镜反应 ③消去反应 ④酯化反应
⑤加成反应 ⑥水解反应
A.②③ B.①②③
C.①④⑤⑥ D.①③④⑥
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列叙述及解释正确的是 ( )
A.2NO2(g)(红棕色)  N2O4(g)(无色) ΔH<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅
N2O4(g)(无色) ΔH<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅
B.对于N2(g)+3H2(g) 2NH3(g),平衡后,保持压强不变,充入Ar,平衡左移
2NH3(g),平衡后,保持压强不变,充入Ar,平衡左移
C.FeCl3+3KSCN Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl固体,因为平衡向逆反应方向移动,故体系颜色变浅
Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl固体,因为平衡向逆反应方向移动,故体系颜色变浅
D.H2(g)+I2(g)  2HI(g) ΔH<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变
2HI(g) ΔH<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 200 ℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+ O2(g)===SO2(g)+H2O(g) ΔH1
O2(g)===SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)=== S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
H2S(g)+ O2(g)===S(g)+H2O(g) ΔH3
O2(g)===S(g)+H2O(g) ΔH3
2S(g)===S2(g) ΔH4
则ΔH4的正确表达式为
A.ΔH4= (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
B.ΔH4= (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4= (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
D.ΔH4= (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列个组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③苯酚钠溶液和CO2
④硝酸银溶液和氨水 ⑤氯化铝溶液和氨水 ⑥碳酸氢钠溶液与澄清石灰水
A. ③⑤ B. ①③⑥ C.仅有⑤ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下方案并进行了实验。

(1)写出沉淀A的化学式___________________________;
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作方法是____________________
_______________________________________________________________________。
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分________(用化学式表示);
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气体为止,既能除去碳酸钠杂质,又能有效地防止新杂质的引入。有关反应的化学方程式为
___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C4H8O3的有机物,在一定条件下具有下列性质:
①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,亦能脱水生成一种只存在一种结构形式,且能使溴水褪色的物质;③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物。根据上述性质,确定 C4H8O3的结构简式为( )
A.HOCH2COOCH2CH3
B.HOCH2CH2CH2COOH
C.CH3CH(OH)CH2CO OH
OH
D.CH3CH2CH(OH)COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸香兰酯是用于调配奶油、冰淇淋的食用香精,其合成反应的化学方程式如下:

下列叙述正确的是( )
A.该反应属于取代反应
B.乙酸香兰酯的分子式为C10H8O4
C.FeCl3溶液可用于区别香兰素与乙酸香兰酯
D.乙酸香兰酯在足量NaOH溶液中水解得到乙酸和香兰素
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
①下列收集Cl2的正确装置是________。

②将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是________。
③设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,____________________________________________________________________________。
(2)能量之间可相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。
限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。

①完成原电池甲的装置示意图(见图),并作相应标注。
要求:在同一烧杯中,电极与溶液含相同的金属元素。
②铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极________。
③甲乙两种原电池中可更有效地将化学能转化为电能的是________,其原因是________________________________________________________________________
________________________。
(3)根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在(2)的材料中应选________作阳极。
查看答案和解析>>
科目:高中化学 来源: 题型:
再生氢氧燃料电池(RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。图为RFC工作原理示意图,下列有关说法正确的是

A.图1把化学能转化为电能,图2把电能转化为化学能,水得到了循环使用
B.a极上发生氧化反应,产生的气体X是H2
C.图2溶液中阳离子从B极流向A极
D.c极上发生的电极反应是O2+2H2O+4e-===4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com