
【题目】用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4 , 过滤;
Ⅱ.向滤液中加入过量MnO2 , 过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度.
(1)步骤Ⅰ中,滤渣的主要成分是
(2)将MnO2氧化Fe2+的离子方程式补充完整: MnO2+ Fe 2++ ═ Mn 2++ Fe 3++
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、 .
(4)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是 .
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度.
已知一定条件下,MnO4﹣与Mn2+反应生成MnO2 . 取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为 .
【答案】
(1)二氧化硅
(2)1;2;4H+;1;2;2H2O
(3)不会引入Cl﹣ , 使制得的MnSO4?H2O产品更纯净
(4)4.7≤a<7.6
(5)![]()
【解析】解:菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4 , 生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,;向滤液中加入过量MnO2 , 将亚铁离子氧化为铁离子,本身被还原为二价锰离子,调节滤液pH,使三价铁离子和铝离子沉淀,过滤除去氢氧化铁和氢氧化铝固体,对硫酸锰溶液进行浓缩、冷切结晶、过滤、洗涤干燥得到产品,(1)菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4 , 生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,滤渣的主要成分是二氧化硅,
所以答案是:二氧化硅;(2)锰元素化合价由+4价降低到+2价,铁元素由+2价升高到+3价,根据化合价升降守恒、电荷守恒、原子守恒,配平反应为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,
所以答案是:1、2+4H+、1、2、2H2O;(3)选用Cl2作为氧化剂会最后的溶液中引入氯离子,使制得的产品不纯,而MnO2不会引入Cl﹣ , 使制得的MnSO4H2O产品更纯净,
所以答案是:不会引入Cl﹣ , 使制得的MnSO4H2O产品更纯净;(4)调节滤液pH,使三价铁离子和铝离子沉淀,根据表格可知二价锰离子开始沉淀的pH=7.6,铝离子开始沉淀的pH=4.7,故4.7≤a<7.6,
所以答案是:4.7≤a<7.6;(5)设含有硫酸锰的物质的量为z,根据方程式
3Mn2+ | + | 2MnO4﹣ | + | 2H2O | = | 5MnO2 | + | 4H+ |
3mol | 2mol | |||||||
z | 0.1y×10﹣3mol |
z=0.15y×10﹣3mol,
锰元素的质量分数= ![]() ,
,
所以答案是: ![]() .
.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】在标准状况下, m g气体A与n g气体B的分子数相同,下列说法中不正确的是
A. 气体A与气体B的相对分子质量比为m∶n
B. 同质量的气体A与B的分子个数比为n∶m
C. 同温同压下,A气体与B气体的密度比为n∶m
D. 同温同压下,同体积的A气体与B气体的质量比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.4 g Al 投入到200.0 mL 2.0 mol·L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为
A. HNO3溶液 B. Ba(OH)2溶液 C. H2SO4溶液 D. HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物分离提纯方法正确的有 ( )
①用萃取法分离溴化钠和单质溴的水溶液 ②用过滤法分离Fe(OH)3胶体和FeCl3溶液的混合物 ③用结晶法提纯混有NaCl的KNO3
A.①②③
B.①③
C.②③
D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学化学原理,解决下列问题:
(1)已知:Si+2NaOH+H2O═Na2SiO3+2H2 . 某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为;
(2)已知:①C(s)+O2(g)═CO2(g)△H=a kJmol﹣1;②CO2(g)+C(s)═2CO(g)△H=b kJmol﹣1;③Si(s)+O2(g)═SiO2(s)△H=c kJmol﹣1 . 工业上生产粗硅的热化学方程式为;
(3)已知:CO(g)+H2O(g)H2(g)+CO2(g).表为该反应在不同温度时的平衡常数.则:该反应的△H0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为 .
温度℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列八种物质: HCl、NH4Cl、N2、Na2O2、CaCl2、Cl2、NaF、CO2。
(1)只含有离子键的物质是______(填化学式,下同)。
(2)既含有离子键,又含有共价键的物质是______。
(3)属于共价化合物的是____,其中所有原子都满足8电子结构的是_____。
(4)写出NaF的电子式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,甲烷的燃烧热是890.3kJmol﹣1 , 则下列热化学方程式书写正确的是( )
A.CH4(g)+ ![]() O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
B.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3kJ?mol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3kJ?mol﹣1
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
已知:①CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206.2kJmol﹣1
②CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式 .
(2)为了探究反应条件对反应CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1的影响,某活动小组设计了三个实验,实验曲线如图所示.
编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
Ⅰ | 530℃ | 3MPa | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅱ | X | Y | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅲ | 630℃ | 5MPa | 1.0molL﹣1 | 3.0molL﹣1 |
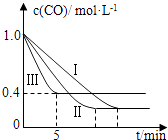
①请依据实验曲线图补充完整表格中的实验条件:X=℃,Y=MPa.
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=molL﹣1min﹣1 .
③实验Ⅱ达平衡时CO的转化率实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往1L容器中投入0.2mol CO(g)、0.2mol H2O(g)、1mol CO2(g)、0.1mol H2(g),此时化学反应将(填“向正方向”、“向逆方向”或“不”) 移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】nmolO2与nmolCO相比较,下列说法不正确的是( )
A. 在同温同压下体积相等
B. 原子数相等
C. 在标准状况下质量相等
D. 分子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com