
| A£®¹żĮæĢś¼ÓČėµ½Ļ”ĻõĖįÖŠ£ŗ 3Fe + 8H+ + 2NO3- = 3Fe2+ + 2NO”ü + 4H2O |
| B£®ĻņNaAlO2ČÜŅŗÖŠĶØČė¹żĮæCO2£ŗ 2AlO2- + CO2+ H2O = 2Al(OH)3”ż+ HCO3- |
| C£®ĻņAgC1Šü×ĒŅŗÖŠµĪ¼Ó±„ŗĶNaIČÜŅŗ: AgC1+I- ="AgI" + C1- |
| D£®ĻņKHCO3ČÜŅŗÖŠ¼ÓČė¹żĮæµÄ³ĪĒåŹÆ»ŅĖ®£ŗ2HCO3-+ Ca2++2OH-=CaCO3”ż+CO32-+2H2O |


 ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®Ļņŗ£“ų»Ņ½ž³öŅŗÖŠ¼ÓČėĮņĖį”¢Ė«ŃõĖ®£ŗ2I-£«2H+£«H2O2 I2£«2H2O I2£«2H2O |
B£®Cuʬ²åČėFeCl3ČÜŅŗÖŠ£ŗCu£«Fe3+ Fe2++Cu2+ Fe2++Cu2+ |
C£®ĻņAl2(SO4)3ČÜŅŗÖŠ¼ÓČė¹żĮæµÄ°±Ė®£ŗ Al3£«£«4NH3”¤H2O  AlO2-£«4NH4+£«2H2O AlO2-£«4NH4+£«2H2O |
| D£®Ļņ NaHSO4ČÜŅŗÖŠµĪ¼ÓBa(OH)2ČÜŅŗÖĮÖŠŠŌ£ŗ |
 BaSO4”ż£«H2O
BaSO4”ż£«H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ģ¼ĖįĒāÄĘČÜŅŗÖŠµĪČėĒāŃõ»ÆøĘČÜŅŗ£ŗHCO3ØD + OHØD £½ CO32ØD£« H2O |
| B£®¶žŃõ»ÆĮņĶØČė“ĪĀČĖįÄĘČÜŅŗ£ŗSO2 + ClOØD + 2OHØD£½ SO42ØD£«ClØD£«H2O |
| C£®Įņ»Æ±µ¼ÓČėĻ”ĮņĖį£ŗBaS + 2H£«£½ H2S”ü+ Ba2+ |
| D£®¹čĖįÄĘČÜŅŗÓė“×ĖįČÜŅŗ»ģŗĻ£ŗSiO32£+2H£«£½H2SiO3”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĢśČÜÓŚĻ”ĻõĖį£¬ČÜŅŗ±ä»Ę: 3 Fe +8H+ +2NO3-="3" Fe2++2NO+4H2O |
| B£®FeBr2ÓėCl2ĪļÖŹµÄĮæÖ®±ČĪŖ1”Ć1Ź±:2Fe2++2Br-+2Cl2=2Fe3++4C1-+Br2 |
| C£®ĻņĆ÷·ÆČÜŅŗÖŠµĪ¼ÓĒāŃõ»Æ±µČÜŅŗÖĮSO42-ĶźČ«³Įµķ:A13++2SO42-+2Ba2++4OH-=2BaSO4”ż+A1O2-+2H2O |
| D£®ĘÆ°×·ŪČÜŅŗÖŠ¼ÓĀČ»ÆĢśČÜŅŗ²śÉś“óĮæŗģŗÖÉ«³Įµķ:Fe3++3C1O-+3H2O=Fe(OH)3”ż+3HC1O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

 2NH3 (g) ”÷H=-38.6kJ”¤mol-1
2NH3 (g) ”÷H=-38.6kJ”¤mol-1| A£®Č«²æ | B£®¢Ś¢Ż | C£®¢Ś¢Ū¢Ü¢ß | D£®¢Ś¢Ü¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®īę£ØCe£©ŌŖĖŲŌŚ×ŌČ»½ēÖŠÖ÷ŅŖŅŌµ„ÖŹŠĪŹ½“ęŌŚ |
| B£®īęČÜÓŚĒāµāĖįµÄ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCe + 4HI = CeI4 + 2H2”ü |
| C£®ÓĆCe£ØSO4£©2ČÜŅŗµĪ¶ØĮņĖįŃĒĢśČÜŅŗ£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗCe4++2Fe2+ = Ce3++2Fe3+ |
D£®ĖÄÖÖĪČ¶ØµÄŗĖĖŲ ”¢ ”¢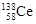 ”¢ ”¢ ”¢ ”¢ £¬ĖüĆĒ»„³ĘĪŖĶ¬Ī»ĖŲ £¬ĖüĆĒ»„³ĘĪŖĶ¬Ī»ĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®“ÅŠŌŃõ»ÆĢśČÜÓŚĒāµāĖį£ŗFe3O4£«8H£« 2Fe3£«£«Fe2£«£«4H2O 2Fe3£«£«Fe2£«£«4H2O |
B£®ÓĆ¹żĮæ°±Ė®ĪüŹÕ¹¤ŅµĪ²ĘųÖŠµÄSO2£ŗ2NH3”¤H2O£«SO2 2NH4£«£«SO32££«H2O 2NH4£«£«SO32££«H2O |
C£®ÓĆÅØŃĪĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗÓė¹żŃõ»ÆĒā·“Ó¦£ŗ2MnO4£ +5H2O2 + 6H+ 2Mn2+ +5O2”ü + 8H2O 2Mn2+ +5O2”ü + 8H2O |
D£®ÓĆ°±Ė®Ļ“µÓŹŌ¹ÜÄŚ±ŚµÄŅų¾µ£ŗAg£«£«2NH3”¤H2O [Ag£ØNH3£©2]++2H2O [Ag£ØNH3£©2]++2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Fe2O3ČÜÓŚ¹żĮæĒāµāĖįČÜŅŗÖŠ£ŗFe2O3 + 6H+ + 2I-=2Fe2+ + I2 +3H2O |
| B£®ĀĮ·ŪÓėNaOHČÜŅŗ·“Ó¦£ŗ2Al + 2OH£=2AlO2£+ H2”ü |
| C£®5.6 g FeÓė200 mL 2.0 mol/L HNO3ČÜŅŗ³ä·Ö·“Ó¦£ŗ3Fe + 2NO3-+ 8H+£½3Fe2+ + 2NO”ü + 4H2O |
D£®Ģ¼ĖįĒāļ§ČÜŅŗÓė×ćĮæµÄNaOHČÜŅŗ»ģŗĻŗó¼ÓČČ£ŗNH4£«£«OH£ NH3”ü£«H2O NH3”ü£«H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®NaHCO3ČÜŅŗĻŌ¼īŠŌ£ŗHCO3-+H2O H3O++CO32- H3O++CO32- |
| B£®ŌŚĆ÷·ÆČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė®£ŗAl3++4NH3·H2O=[Al(OH)4]-+4NH4+ |
| C£®ĻŌĄ¶É«µÄµķ·ŪČÜŅŗÖŠĶØČėSO2ŗó±ä³ÉĪŽÉ«ČÜŅŗ£ŗI2 +SO2+2H2O=2I-+SO42-+4H+ |
| D£®Š”ĖÕ“ņČÜŅŗÖŠ¼ÓÉŁĮæBa(OH)2ČÜŅŗ£ŗHCO3-+Ba2++OH-=BaCO3”ż+H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com