
ة╛╠ظ─┐ة┐LEDثذLight Emitting Diodeثرثش╖ت╣ظ╢■╝س╣▄ثش╩╟╥╗╓╓─▄╣╗╜س╡ق─▄╫ز╗»╬ز┐╔╝√╣ظ╡─╣╠╠ش╡─░ن╡╝╠ف╞≈╝■ثش╦ⁿ┐╔╥╘╓▒╜╙░╤╡ق─▄╫ز╗»╬ز╣ظ─▄ةث╧┬═╝╩╟┐╬═ظ╗ى╢»╨ة╫ل╔ك╝╞╡─╙├╗»╤د╡ق╘┤╩╣LED╡╞╖ت╣ظ╡─╫░╓├ةث╧┬┴╨╦╡╖ذ┤و╬ٍ╡─╩╟
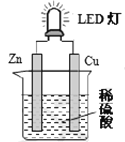
Aث«╫░╓├╓╨┤µ╘┌ة░╗»╤د─▄ة·╡ق─▄ة·╣ظ─▄ة▒╡─╫ز╗╗
Bث«═ص╞ش╔╧╖ت╔·╡─╖┤╙خ╬زث║2Hثس+2eذDث╜H2ةⁿ
Cث«╚ق╣√╜س┴ٌ╦ط╗╗│╔─√├╩╓صثش╡╝╧▀╓╨▓╗╗ط╙╨╡ق╫╙┴≈╢»
Dث«╚ق╣√╜س╨┐╞ش╗╗│╔╠·╞شثش╡ق┬╖╓╨╡─╡ق┴≈╖╜╧ٌ▓╗▒غ
ة╛┤≡░╕ة┐C
ة╛╜ظ╬ِة┐
╩╘╠ظ╖╓╬ِث║Aث«╘ص╡ق│╪░╤╗»╤د─▄╫ز╗»╬ز╡ق─▄ثش╡ق─▄╙╓╫ز╗»╬ز╣ظ─▄ثش╝┤╫░╓├╓╨┤µ╘┌ة░╗»╤د─▄ة·╡ق─▄ة·╣ظ─▄ة▒╡─╫ز╗╗ثشA╒²╚╖ث╗Bث«╨┐╡─╜≡╩َ╨╘╟┐╙┌═صثش╨┐╩╟╕║╝سثش═ص╩╟╒²╝سثش╚▄╥║╓╨╡─└ن╫╙╘┌╒²╝س╖┼╡قثش╝┤═ص╞ش╔╧╖ت╔·╡─╖┤╙خ╬زث║2Hثس+2eذDث╜H2ةⁿثشB╒²╚╖ث╗Cث«╚ق╣√╜س┴ٌ╦ط╗╗│╔─√├╩╓صثش╚╘╚╗┐╔╥╘╣╣│╔╘ص╡ق│╪ثش╥ٌ┤╦╡╝╧▀╓╨╗ط╙╨╡ق╫╙┴≈╢»ثشC┤و╬ٍث╗Dث«╚ق╣√╜س╨┐╞ش╗╗│╔╠·╞شثش╚╘╚╗╩╟═ص╫≈╒²╝سثش╠·╫≈╕║╝سثش╝┤╡ق┬╖╓╨╡─╡ق┴≈╖╜╧ٌ▓╗▒غثشD╒²╚╖ثش┤≡░╕╤ةCةث



| ─م╝╢ | ╕▀╓╨┐╬│╠ | ─م╝╢ | │ُ╓╨┐╬│╠ |
| ╕▀╥╗ | ╕▀╥╗├ظ╖╤┐╬│╠═╞╝ِثة | │ُ╥╗ | │ُ╥╗├ظ╖╤┐╬│╠═╞╝ِثة |
| ╕▀╢■ | ╕▀╢■├ظ╖╤┐╬│╠═╞╝ِثة | │ُ╢■ | │ُ╢■├ظ╖╤┐╬│╠═╞╝ِثة |
| ╕▀╚² | ╕▀╚²├ظ╖╤┐╬│╠═╞╝ِثة | │ُ╚² | │ُ╚²├ظ╖╤┐╬│╠═╞╝ِثة |
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐┴ٌ╡ح╓╩║═╗»║╧╬ي╘┌╣ج┼ر╥╡╔·▓·╓╨╙╨╫┼╓╪╥ز╡─╙خ╙├ثش╢°SO2╓▒╜╙┼┼╖┼╗ط╢╘╗╖╛│╘ه│╔╬ث║خةث
تً.SO2╡─╬▓╞°┤خ└و═ذ│ث╙╨╥╘╧┬╝╕╓╓╖╜╖ذث║
ثذ1ثر╗ى╨╘╠┐╗╣╘ص╖ذ ╖┤╙خ╘ص└وث║║ع╬┬║ع╚▌╩▒2C(s)+2SO2(g)![]() S2(g)+2CO2(g)ةث╖┤╙خ╜°╨╨╡╜▓╗═ش╩▒╝غ▓ظ╡├╕≈╬ي╓╩╡─┼ذ╢╚▓┐╖╓═╝╧ٍ╚ق═╝ث║
S2(g)+2CO2(g)ةث╖┤╙خ╜°╨╨╡╜▓╗═ش╩▒╝غ▓ظ╡├╕≈╬ي╓╩╡─┼ذ╢╚▓┐╖╓═╝╧ٍ╚ق═╝ث║

ت┘0ةس20 min╖┤╙خ╦┘┬╩▒و╩╛╬زv(SO2)=________ث╗
ت┌30 min╩▒ثش╕─▒غ─│╥╗╠ُ╝■╞╜║ظ╖ت╔·╥╞╢»ثش╘ٌ╕─▒غ╡─╠ُ╝■╫ى╙╨┐╔─▄╩╟________ث╗
ت█40 min╩▒ثش╞╜║ظ│ث╩²K=________ةث
ثذ2ثر╤╟┴ٌ╦ط─╞╬ⁿ╩╒╖ذ ت┘Na2SO3╚▄╥║╬ⁿ╩╒SO2╡─└ن╫╙╖╜│╠╩╜╬ز__________________ث╗
ت┌│ث╬┬╧┬ثش╡▒╬ⁿ╩╒╓┴NaHSO3╩▒ثش╬ⁿ╩╒╥║╓╨╧ض╣╪└ن╫╙┼ذ╢╚╣╪╧╡╥╗╢ذ╒²╚╖╡─╩╟___(╠ى╨ٌ║┼)ةث
aث«c(Na+)+c(H+)>c(![]() )+c(
)+c(![]() )+c(OH)
)+c(OH)
bث«╦«╡ق└ن│ِc(H+)=1ة┴108 mol/L
cث«c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() )
)
ثذ3ثر╡ق╗»╤د┤خ└و╖ذ

ت┘╚ق═╝╦∙╩╛ثشPt(تً)╡ق╝س╡─╖┤╙خ╩╜╬ز__________________ث╗
ت┌╡▒╡ق┬╖╓╨╫ز╥╞0.02 mol e╩▒(╜╧┼ذH2SO4╔╨╬┤┼┼│ِ)ثش╜╗╗╗─ج╫ٍ▓ض╚▄╥║╓╨╘╝╘ِ╝╙____mol└ن╫╙ةث
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╨┬╛╔╢»─▄╫ز╗╗╣ج│╠╓«╥╗╩╟╨┬─▄╘┤╨┬▓─┴╧╡─═┌╛ٌ║═╙خ╙├ةث╥╥╢■┤╝╩╟╓╪╥ز╡─╗»╣ج╘ص┴╧ثش ├║╗∙║╧│╔╞°(COةت H2)╝غ╜╙╓╞╥╥╢■┤╝╛▀╙╨╫ز╗»┬╩╕▀ةت╗╪╩╒┬╩╕▀╡╚╙┼╡عثش╩╟╬╥╣·╥╗╧ى╙╡╙╨╫╘╓≈╓ز╩╢▓·╚ذ╡─╩└╜ق╩╫┤┤╝╝╩ُثش╓╞▒╕╣²│╠╚ق╧┬ث║
╖┤╙خ I: 4NO(g)+4CH3OH(g)+O2(g) ![]() 4CH3ONO(g)+2H2O(g) ة≈H1 = a kJةجmol-1
4CH3ONO(g)+2H2O(g) ة≈H1 = a kJةجmol-1
╖┤╙خ II: 2CO(g)+2CH3ONO(g) ![]() CH3OOCCOOCH3(l) + 2NO(g) ة≈H2= b kJةجmol-1
CH3OOCCOOCH3(l) + 2NO(g) ة≈H2= b kJةجmol-1
╖┤╙خ III: CH3OOCCOOCH3(1)+4H2(g) ![]() HOCH2CH2OH(1)+2CH3OH(g) ة≈H3= c kJةجmol-1
HOCH2CH2OH(1)+2CH3OH(g) ة≈H3= c kJةجmol-1
ثذ1ثر╟ن╨┤│ِ├║╗∙║╧│╔╞°[n(CO): n(H2)= 1:2]╙ن╤ُ╞°╝غ╜╙║╧│╔╥╥╢■┤╝╡─╫▄╚╚╗»╤د╖╜│╠╩╜________ثش╥╤╓ز╕├╖┤╙خ╘┌╜╧╡═╬┬╠ُ╝■╧┬─▄╫╘╖ت╜°╨╨ثش╘ٌ╕├╖┤╙خ╡─ة≈H ____0(╠ىة░>ة▒ة░<ة▒╗ٌة░=ة▒)ةث
ثذ2ثر╥╗╢ذ╬┬╢╚╧┬ثش╘┌ 2 L ╡─├▄▒╒╚▌╞≈╓╨═╢╚ن╬ي╓╩╡─┴┐╛∙╬ز 0.4mol╡─CO ║═ CH3ONO╖ت╔·╖┤╙خ IIثش10min ┤ي╡╜╞╜║ظ╩▒CO╡─╠ف╗²╖╓╩²╙نNO╡─╠ف╗²╖╓╩²╧ض╡╚ةث
ت┘╧┬┴╨╤ة╧ى─▄┼╨╢╧╖┤╙خ╥╤┤ي╡╜╗»╤د╞╜║ظ╫┤╠ش╡─╩╟________ةث
a. CO ╡─╓╩┴┐▓╗╘┘▒غ╗» b. ╗ه║╧╞°╠ف╡─├▄╢╚▓╗╘┘▒غ╗»
c.╡ح╬╗╩▒╝غ─┌╔·│╔ CO ║═ NO ╡─╬ي╓╩╡─┴┐╧ض╡╚ d. CO ║═ CH3ONO ╡─┼ذ╢╚▒╚▓╗╘┘▒غ╗»
ت┌10min ─┌╕├╖┤╙خ╡─╦┘┬╩ خ═(NO)=____________ث╗╕├╬┬╢╚╧┬╗»╤د╞╜║ظ│ث╩² K=_________ةث╚َ┤╦╩▒╧ٌ╚▌╞≈╓╨╘┘═ذ╚ن0.4 mol NOثش╥╗╢╬╩▒╝غ║ٍثش┤ي╡╜╨┬╞╜║ظ╩▒ NO╡─╠ف╗²╖╓╩²╙ن╘ص╞╜║ظ╩▒╧ض▒╚______(╠ىة░╘ِ┤ٍة▒ة░╧ض╡╚ة▒ة░╝ُ╨ةة▒╗ٌة░▓╗─▄╚╖╢ذة▒)ةث
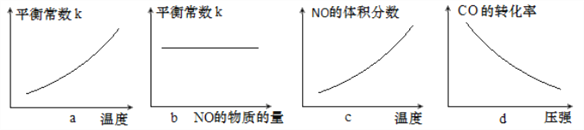
ت█╚َ╕├╖┤╙خة≈Hث╝0ثش╘┌║ع╚▌╡─├▄▒╒╚▌╞≈╓╨ثش╖┤╙خ┤ي╞╜║ظ║ٍثش╕─▒غ─│╥╗╠ُ╝■ثش╧┬┴╨╩╛╥ظ═╝╒²╚╖╡─╩╟____________ثذ╠ى╫╓─╕ثرةث
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╧┬┴╨╩╡╤ل▓┘╫≈╓╨ثش▓╗║╧└و╡─╩╟( )

A. ╧┤╡╙│┴╡و╩▒(╚ق═╝ت┘)ثش╧ٌ┬ر╢╖╓╨╝╙╩╩┴┐╦«ثش╜┴░ك▓ت┬╦╕╔
B. ╙├CCl4╠ط╚ة╡ظ╦«╓╨╡─╡ظثش╤ةت█
C. ╒َ┴ٍ╩▒╒َ┴ٍ╔╒╞┐╓╨╥║╠ف╡─╠ف╗²▓╗─▄│ش╣²╚▌╗²╡─2/3ثش╥║╠ف╥▓▓╗─▄╒َ╕╔
D. ┤╓╤╬╠ط┤┐ثش╤ةت┘║═ت┌
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╙├0.1 mol / L╡─Na2SO3╚▄╥║30 mLثش╟ة║├╜س2ة┴10ثص3 mol╡─XO4ثص└ن╫╙╗╣╘صثش╘ٌ╘ز╦╪X╘┌╗╣╘ص▓·╬ي╓╨╡─╗»║╧╝█╩╟ ( )
A.ثس1B.ثس2C.ثس3D.ثس4
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐┤╬┴ٌ╦ط╟ظ─╞╝╫╚ر(NaHSO2ةجHCHOةج2H2O)╦╫│╞╡ُ░╫┐لثش▓╗╬╚╢ذثش120ةµ╩▒╗ط╖╓╜ظثش╘┌╙ة╚╛ةت ╥╜╥ر╥╘╝░╘ص╫╙─▄╣ج╥╡╓╨╙╨╣ع╖║╙خ╙├ةث╥╘ Na2SO3ةتSO2ةتHCHO ║═╨┐╖█╬ز╘ص┴╧╓╞▒╕┤╬┴ٌ╦ط╟ظ─╞╝╫╚ر╡─ ╩╡╤ل╫░╓├╚ق╧┬═╝╦∙╩╛ث║

╩╡╤ل▓╜╓كث║
▓╜╓ك 1ث║╘┌╚²╛▒╔╒╞┐╓╨╝╙╚ن╥╗╢ذ┴┐ Na2SO3 ║═╦«ثش╜┴░ك╚▄╜ظثش
╗║┬²═ذ╚ن SO2ثش╓┴╚▄╥║ pH ╘╝╬ز 4ثش╓╞╡├ NaHSO3 ╚▄╥║ث╗
▓╜╓ك 2ث║╜س╫░╓├ A ╓╨╡╝╞°╣▄╗╗│╔╧≡╞ج╚√ةث╧ٌ╔╒╞┐╓╨╝╙╚ن╔╘╣²┴┐ ╡─╨┐╖█║═╥╗╢ذ┴┐╝╫╚ر╚▄╥║ثش╘┌ 80ةس90ةµ╧┬ثش╖┤╙خ╘╝ 3hثش└غ╚┤ ╓┴╩╥╬┬ثش│ل┬╦ث╗
▓╜╓ك 3ث║╜س┬╦╥║╒µ┐╒╒َ╖ت┼ذ╦ُثش└غ╚┤╜ط╛دةث
ثذ1ثر╫░╓├ B ╡─╔╒▒ص╓╨╙خ╝╙╚ن╡─╚▄╥║╩╟____________ث╗└غ─²╣▄╓╨└غ╚┤╦«┤╙____________(╠ىة░aة▒╗ٌة░bة▒)┐┌╜° ╦«ةث
ثذ2ثرA ╓╨╢ض┐╫╟ٌ┼▌╡─╫≈╙├╩╟____________ةث
ثذ3ثر╨┤│ِ▓╜╓ك 2 ╓╨╖ت╔·╖┤╙خ╡─╗»╤د╖╜│╠╩╜____________ةث
ثذ4ثر▓╜╓ك 3 ╓╨╘┌╒µ┐╒╚▌╞≈╓╨╒َ╖ت┼ذ╦ُ╡─╘ص╥ٌ╩╟╩╟╖└╓╣╬┬╢╚╣²╕▀╩╣▓·╬ي╖╓╜ظثش╥▓╖└╓╣____________ةث
ثذ5ثر╬ز┴╦▓ظ╢ذ▓·╞╖╡─┤┐╢╚ثش╫╝╚╖│╞╚ة 2.0g ╤∙╞╖ثش═م╚س╚▄╙┌╦«┼غ│╔ 100mL ╚▄╥║ثش╚ة 20.00mL ╦∙┼غ╚▄ ╥║ثش╝╙╚ن╣²┴┐╡ظ═م╚س╖┤╙خ║ٍ(╥╤╓ز I2 ▓╗─▄╤ُ╗»╝╫╚رثش╘╙╓╩▓╗╖┤╙خ)ثش╝╙╚ن BaCl2 ╚▄╥║╓┴│┴╡و═م╚سثش╣² ┬╦ةت╧┤╡╙ةت╕╔╘ي╓┴║ع╓╪╡├╡╜░╫╔س╣╠╠ف 0.466gةثM(NaHSO2ةجHCHOةج2H2O)=154g/mol]
ت┘╚ق║╬╝ه╤ل│┴╡و╩╟╖ً╧┤╛╗____________ةث
ت┌╘ٌ╦∙╓╞╡├╡─▓·╞╖╡─┤┐╢╚╬ز____________ةث
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╠╜╛┐Na2S2O3+H2SO4=Na2SO4+SO2ةⁿ+Sة²+H2O ╖┤╙خ╡─╦┘┬╩╙░╧ه╥ٌ╦╪ثش╔ك╝╞┴╦╥╘╧┬╩╡╤لثش╧┬┴╨╦╡╖ذ╒²╚╖╡─╩╟
╫╢╨╬╞┐ | 0.1molLNa2S2O3 ╚▄╥║/mL | ╒َ┴ٍ╦« | 0.2mol/L H2SO4 ╚▄╥║ | ╖┤╙خ╬┬╢╚ | ╗ن╫╟│ِ╧╓╩▒╝غ/s | ▒╕╫ت |
1 | 10 | 0 | 10 | 20ةµ | 10 | |
2 | 10 | 5 | 5 | 20ةµ | 16 | |
3 | 10 | 0 | 10 | 50ةµ | 5 | ╡┌10 ├ن┐ز╩╝╗ن╫╟▓╗╘┘╘ِ╢ض |
4 | 10 | 6 | 4 | 50ةµ | 8 |
A. ╕├╖┤╙خ╥▓┐╔═ذ╣²▓ظSO2╡─╠ف╗²▒غ╗»└┤▒و╩╛╗»╤د╖┤╙خ╦┘┬╩╡─┐ه┬²
B. 3║┼╞┐╙├Na2S2O3 └┤▒و╩╛╦┘┬╩╬ز0ث«0lmol/(Ls)
C. ╙╔2║┼╞┐║═3║┼╞┐╩╡╤ل╜ط╣√┐╔╡├╬┬╢╚╘╜╕▀╖┤╙خ╦┘┬╩╘╜┐ه
D. ╙╔1║┼╞┐║═4║┼╞┐╩╡╤ل╜ط╣√┐╔╡├╬┬╢╚╘╜╕▀╖┤╙خ╦┘┬╩╘╜┐ه
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╥╤╓ز─│╢╠╓▄╞┌╘ز╦╪╘ص╫╙╡─╡┌╚²╡ق╫╙▓ع╔╧┼┼▓╝╙╨5╕ِ╡ق╫╙ثش╘ٌ╕├╘ز╦╪╘┌╓▄╞┌▒و╓╨╡─╬╗╓├╩╟ثذ ثر
A.╡┌╢■╓▄╞┌تَA╫ف
B.╡┌╢■╓▄╞┌تُA╫ف
C.╡┌╚²╓▄╞┌تَA╫ف
D.╡┌╚²╓▄╞┌تُA╫ف
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
┐╞─┐ث║╕▀╓╨╗»╤د └┤╘┤ث║ ╠ظ╨═ث║
ة╛╠ظ─┐ة┐╙╨╣╪╙═╓ش║═╠╟└ض╡─╦╡╖ذ╒²╚╖╡─╩╟
A. ╢╝─▄╚▄╙┌╦« B. ╢╝╩╟╕▀╖╓╫╙╗»║╧╬ي
C. ╢╝┐╔╥╘╦«╜ظ D. ╢╝║ش╙╨CةتHةتO╚²╓╓╘ز╦╪
▓ل┐┤┤≡░╕║═╜ظ╬ِ>>
░┘╢╚╓┬╨┼ - ┴╖╧░▓ط┴╨▒و - ╩╘╠ظ┴╨▒و
║■▒▒╩ة╗ح┴ز═°╬ح╖ذ║═▓╗┴╝╨┼╧ت╛┘▒ذ╞╜╠ذ | ═°╔╧╙╨║خ╨┼╧ت╛┘▒ذ╫ذ╟° | ╡ق╨┼╒ر╞ص╛┘▒ذ╫ذ╟° | ╔µ└·╩╖╨ل╬▐╓≈╥ف╙╨║خ╨┼╧ت╛┘▒ذ╫ذ╟° | ╔µ╞ٍ╟╓╚ذ╛┘▒ذ╫ذ╟°
╬ح╖ذ║═▓╗┴╝╨┼╧ت╛┘▒ذ╡ق╗░ث║027-86699610 ╛┘▒ذ╙╩╧غث║58377363@163.com