
【题目】某有机物A的红外光谱和核磁共振氢谱图如图所示,下列说法中错误的是( ) 
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.若A的化学式为C2H6O,则其结构简式为CH3﹣O﹣CH3
C.仅由其核磁共振氢谱图无法得知其分子中的氢原子总数
D.由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子
【答案】B
【解析】解:A.红外光谱可知分子中至少含有C﹣H键、C﹣O键、O﹣H键三种不同的化学键,故A正确;
B.若A的化学式为 C2H60,CH3﹣O﹣CH3中只有一种氢原子,所以其吸收峰个数应该是1,与图象不符合,故B错误;
C.核磁共核磁共振氢谱中有3个峰说明分子中3种H原子,故C正确;
D.振氢谱中只能确定H原子种类,不能确定氢原子总数,故D正确;
故选B.
A.由红外光谱可知,该有机物中C﹣H、C﹣O、O﹣H三种化学键;
B.由红外光谱可知分子中含有C﹣H键、C﹣O键、O﹣H键结合分子得出结构简式;
C.核磁共振氢谱中有几个峰就有几种H原子,只能确定H原子种类;
D.核磁共振氢谱中有几个峰就有几种H原子,峰的面积之比等于H原子数目之比.


科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下表所示:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(1)单质铜和元素M的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式为________________________________________________________________________。
(2)元素Q、元素Z的含量影响钢铁性能,采用下图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。
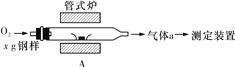
①气体a的成分是________________(填化学式)。
②若钢样中元素Z以FeZ的形式存在,在装置A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是:______________________________________________。
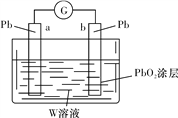
(3)用Z的最高价含氧酸W的溶液作电解质溶液(体积为1 L,假设反应前后溶液体积变化忽略不计)组装成原电池(如图所示)。则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W溶液的浓度由质量分数39%(密度为1.3 g/cm3)变为______mol/L(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组欲进行如下实验探究金属与浓硫酸反应。试回答下列问题。
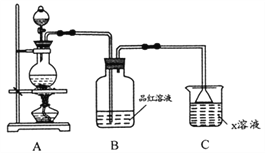
(1)利用上图装置研究铜与浓硫酸反应,反应化学方程式为_________;B装置的目的是______;x溶液为___________。
(2)将上述实验中的铜改为黄铜(铜锌合金),实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快。该气体可能为____,气体产生越来越快的原因可能是_____(至少两点)。验证该气体的实验方案如下:
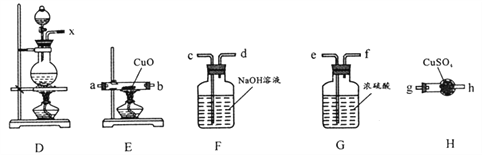
①装置连接顺序:x→_________;
②能证明上述假设成立的实验现象是__________。
(3)取少量镁粉加入盛浓硫酸的烧杯,在通风橱中实验。充分反应后溶液中有灰白色悬浮物,设计方案研究该悬浮物的组成,请帮助完善。(假设镁的化合物都溶于稀酸)
![]() _____
_____
写出产生该灰白色悬浮物主要反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。一定条件下,恒容密闭容器中,发生反应:CO(g)+2H2(g) ![]() CH3OH(g) 。下列能充分说明该反应已经达到化学平衡状态的是
CH3OH(g) 。下列能充分说明该反应已经达到化学平衡状态的是
A. 正、逆反应速率都等于零 B. CO、H2、CH3OH的浓度不再变化
C. CO、H2、CH3OH的浓度相等 D. CO、H2、CH3OH在密闭容器中共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究题
Ⅰ.某烃A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢.
(1)写出A的结构简式 .
(2)A中的碳原子是否都处于同一平面?(填“是”或者“不是”).
(3)Ⅱ.2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.“亮菌甲素”的结构简式为: 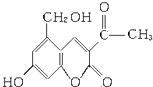
它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
①下列有关“亮菌甲素”的叙述正确的是(填字母).
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素”的分子式是C12H10O5
D.“亮菌甲素”分子中含氧官能团只有2种
②丙二醇的分子式是C3H8O2 , 已知两个羟基连在同一个碳原子上的物质不存在.写出其所有属于醇类的同分异构体的结构简式.
③依据核磁共振氢谱分析,二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1.又知二甘醇中含碳、氧元素的质量分数相同,且氢元素的质量分数为9.4%,1mol二甘醇与足量金属钠反应生成1mol H2 . 写出二甘醇的结构简式. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869 年,俄国化学家门捷列夫制作出了第一张元素周期表,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表含元素最多的族是第ⅢB 族
B.元素周期表有 18 个族
C.第ⅠA 族的元素全部都是金属元素
D.短周期是指第一、二、三、四周期
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com