
为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚.为检验驾驶员是否酒后驾车,可采用的检验方法有多种.回答以下问题:
(1)早期曾经采用五氧化二碘和某种高分子化合物X的混合溶液来检测酒精的存在.其原理是:I
2O
5与CH
3CH
2OH先发生反应(I
2O
5+5CH
3CH
2OH=I
2+5Y+5H
2O),生成的I
2与高分子化合物X作用而变蓝.交警依据此原理来检测驾驶员是否饮酒.则:X的化学式是
(C6H10O5)n
(C6H10O5)n
;Y的化学式是
C2H4O(或CH3CHO)
C2H4O(或CH3CHO)
;
(2)已知:I
2O
5是白色固体,可用于检验并定量测定空气中CO;两者在常温条件下发生的反应为5CO+I
2O
5=5CO
2+I
2(空气中其余气体不与I
2O
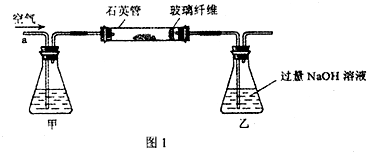
5反应);某同学设计如右实验装置完成上述目的.
①指出能证明空气中有CO存在的现象.答:
玻璃管中白色固体变为紫黑色
玻璃管中白色固体变为紫黑色
.
②将上述反应生成的碘单质用硫代硫酸钠滴定(反应为I
2+2Na
2S
2O
3=Na
2S
4O
6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量.若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗vmL c mol?L
-1Na
2S
2O
3溶液.则该空气样品中CO的体积分数是
.
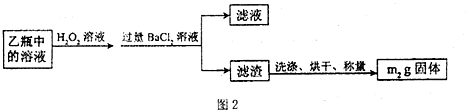
③有同学提出只要依据参与反应的空气体积和洗气瓶中白色沉淀的质量也可求得空气中CO.此方案是否可行?
答:
不可行
不可行
.
(3)燃料电池酒精检测仪(该电池以硫酸溶液为电解质溶液)也是检测酒精含量的一种方法.总反应是:CH
3CH
2OH+O
2=CH
3COOH+H
2O.该电池负极电极反应式是
CH3CH2OH+H2O-4e-=CH3COOH+4H+
CH3CH2OH+H2O-4e-=CH3COOH+4H+
.
(4)酒精是一种较为环保的燃料,298K时,1g乙醇完全燃烧放出热量qkJ,写出乙醇燃烧的热化学方程式
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-46qkJ/mol
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-46qkJ/mol
.



 为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚.为检验驾驶员是否酒后驾车,可采用的检验方法有多种.回答以下问题:
为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚.为检验驾驶员是否酒后驾车,可采用的检验方法有多种.回答以下问题:![]() A. B.
A. B.![]() C.
C.![]()
![]() D.
D.