
һ���¶��£����淴Ӧ2NO2(g)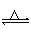
 2NO(g)��O2(g)������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��(����)
2NO(g)��O2(g)������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��(����)
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2��ͬʱ����2n mol NO
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1
�ܻ�������ѹǿ���ٸı�
�ݻ���������ɫ���ٸı�
��������ƽ����Է����������ٸı䡡��������������������������������
A���٢ܢݢ� B���٢ڢۢ� C���ڢۢܢ� D������ȫ��
A��[������n mol O2����������2n mol NO2��������NO2�����ʵ�������NO2�����ʣ��ܱ�ʾv����v�棬��ȷ���ڱ�ʾͬһ����ķ�Ӧ���ʣ����ܱ�ʾv����v�棬����ȷ����ֻҪ������Ӧ������˵���۷�Ӧ�Ƿ�ﵽƽ�⣬NO2��NO��O2�ķ�Ӧ����֮�Ⱦ�Ϊ2��2��1�������ܷ�ӳ���淴Ӧ�Ƿ�ﵽƽ�⣬����ȷ�����¶ȡ����һ�����������ѹǿ���ٸı䣬���ڷ�Ӧǰ�������������ȵķ�Ӧ��˵������������ʵ������ٸı䣬�����Ѵ�ƽ�⡣����ɫ����dz��������ɫ����NO2��Ũ�ȣ����������ɫ���䣬˵��NO2��Ũ�Ȳ��ٸı䣬��˵���Ѵﵽƽ�⣬��ȷ����������ƽ����Է�������( ��
��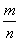 )���䣬˵������������ʵ���(n)���䣬�����Ѵ�ƽ�⣬��ȷ��
)���䣬˵������������ʵ���(n)���䣬�����Ѵ�ƽ�⣬��ȷ��
����������жϿ��淴Ӧ�Ƿ�ﵽ��ѧƽ��״̬�����ݺͷ���
���淴Ӧ�ﵽ��ѧƽ��״̬ʱ��������Ҫ��������һ������Ӧ���ʺ��淴Ӧ������ȣ����Ƿ�Ӧ������и���ɵ�����(��Ũ��)���ֲ��䡣���������������жϿ��淴Ӧ�Ƿ�ﵽ��ѧƽ��״̬�ĺ��������ݡ����淴Ӧ�߱��������ص�֮һ�����ʹﵽ�˻�ѧƽ��״̬�����淴Ӧ���߱������������е��κ�һ��������δ�ﵽ��ѧƽ��״̬��]



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪H2(g)��Cl2(g)===2HCl(g)����H����184.6 kJ��mol��1����Ӧ��HCl(g)===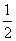 H2(g)��
H2(g)��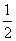 Cl2(g)�Ħ�HΪ (����)��
Cl2(g)�Ħ�HΪ (����)��
A����184.6 kJ��mol��1�� B����92.3 kJ��mol��1
C����369.2 kJ��mol��1�� D����92.3 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ϩ����������ȩ����Ƴ�����ͼ��ʾ��ȼ�ϵ�أ�
�����Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦΪ��
2CH2��CH2 +O2��2CH3CHO�������й�˵����ȷ����
A��ÿ��0.1mol O2��Ӧ����Ǩ��H+ 0.4mol
B��������ӦʽΪ��CH2��CH2��2e- + 2OH- = CH3CHO + H2O
C�������ƶ����缫a��������Һ���缫b D���õ��Ϊ�ɳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ�������ֵ������������ȷ����(����)
A����״���£�2.24 Lˮ��������������ΪNA
B��1 L 0.2 mol��L��1��������Һ�к��е�SO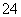 ��ĿΪ0.6NA
��ĿΪ0.6NA
C��1 mol���ͱ�����Ļ������ȫȼ��ʱ����O2�ķ�����Ϊ7.5NA
D����״���£�7.1 g����������ʯ�����ַ�Ӧת�Ƶ�����Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£���ӦA2(g)��B2(g)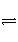
 2AB(g)�ﵽƽ��ı�־��(����)
2AB(g)�ﵽƽ��ı�־��(����)
A����λʱ��������n mol��A2��ͬʱ����n mol��AB
B�������ڵ���ѹǿ����ʱ��ı仯���仯
C����λʱ��������2n mol��ABͬʱ����n mol��B2
D��ƽ����Է�����������ʱ��仯���仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳɾ۱�ϩ����ά�ĵ����DZ�ϩ�棬���������������ַ����Ʊ���
����һ��CaCO3 CaO
CaO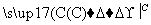 CaC2
CaC2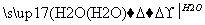 CH��CH
CH��CH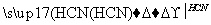 CH2===CH—CN
CH2===CH—CN
��������CH2===CH—CH3��NH3��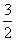 O2
O2 CH2===CH—CN��3H2O
CH2===CH—CN��3H2O
�ٷ������ȷ���һ��Ӧ�����٣���Դ���ĵͣ��ɱ��͡��ڷ������ȷ���һԭ�Ϸḻ�����ռ��۷������ȷ���һ�������ж������ʹ�ã���������Ⱦ���ܷ�������Ҫ��Ӧ�¶ȸߣ����ܴ�
�������������ַ���������ȷ����(����)
A���٢ڢ� B���٢ۢ�
C���ڢۢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijǿ������ҺX�п��ܺ���NH ��Fe2����Al3����CO
��Fe2����Al3����CO ��SO
��SO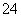 ��Cl����NO
��Cl����NO �е������֡�ij�о���ѧϰС��Ϊ̽����ҺX����ɣ���������ʵ��(����YΪ��ɫ��ζ������)��
�е������֡�ij�о���ѧϰС��Ϊ̽����ҺX����ɣ���������ʵ��(����YΪ��ɫ��ζ������)��

�ش��������⣺
(1)��ҺX�п϶����ڵ�������__________________���϶������ڵ�������____________________________________________________��
(2)д����������A�����ӷ���ʽ��____________________________________ _________________________________________________________________��
(3)д������ҺE��ͨ������Yһ�����������ӷ���ʽ��___________________ _________________________________________________________________��
(4)�������ʵ�鷽����һ��ȷ�����ܴ��ڵ����ӣ�д��ʵ��IJ������衢��������ۣ�_________________________________________________________ _________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ�У�Fe2+�ᱻ������������ΪFe3+����ͬ�����£�һ��Ũ�ȵ�Fe2+����������ʱ��仯��ϵ����ͼ��ʾ�������й�˵����ȷ����
A�����������̵����ӷ���ʽΪ��
Fe2++O2+4H+===Fe3++2H2O
B��pH=1.5ʱFe2+��������һ����pH=2.5�Ĵ�
C��Fe2+�������ʽ�����Һ��pH���¶��й�
D������������ͬʱ��80��ʱFe2+�������ʱ�50��Ĵ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com