
һ���¶��£��п��淴Ӧ��2A��g��+2B��g�� C��g��+3D��g������H��0���ֽ�2 mol A��2 mol B�������ΪV�ļ���������2 mol C��6 mol D������������ʹ�������ڷ�Ӧ��ʼǰ�����Ϊ2V����ͼ1����
C��g��+3D��g������H��0���ֽ�2 mol A��2 mol B�������ΪV�ļ���������2 mol C��6 mol D������������ʹ�������ڷ�Ӧ��ʼǰ�����Ϊ2V����ͼ1����
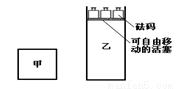
�����������з�Ӧ��˵����ȷ����
A����������ƽ���������ͬ���¶�ʱ���������ķ�Ӧ���ʴ���������������
B���������еķ�Ӧ����ƽ��ʱ��ƽ�������и���ݵ�����ٷ������ͬ�����������ܶȲ�ͬ
C���������еķ�Ӧ�ȴﵽ��ѧƽ��״̬
D���ڼ��������ٳ���2mol A��2 mol B��ƽ����������C�����ʵ�������������C�����ʵ�����2��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16O��18O��Ϊͬλ�� | B�� | 16O��18O���в�ͬ�ĵ����� | ||
| C�� | 16O��18O��Ϊͬ�������� | D�� | 16O��18O��ѧ���ʲ�ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ������
�ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��ΪN2(g)��3H2(g)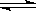 2NH3(g) ��H����92.4 kJ��mol��1��һ�ֹ�ҵ�ϳɰ��ļ�ʽ����ͼ���£�
2NH3(g) ��H����92.4 kJ��mol��1��һ�ֹ�ҵ�ϳɰ��ļ�ʽ����ͼ���£�
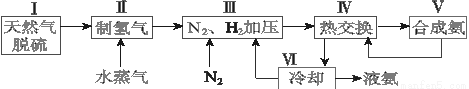
(1)��Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽ��_______________��
(2)���������������ԭ�����£�
��CH4(g)��H2O(g)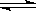 CO(g)��3H2(g) ��H����206.4 kJ��mol��1
CO(g)��3H2(g) ��H����206.4 kJ��mol��1
��CO(g)��H2O(g)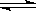 CO2(g)��H2(g) ��H����41.2 kJ��mol��1
CO2(g)��H2(g) ��H����41.2 kJ��mol��1
���ڷ�Ӧ�٣�һ���������ƽ����ϵ��H2�İٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ�� __��
���÷�Ӧ�ڣ���CO��һ��ת���������H2�IJ�������1 mol CO��H2�Ļ������(CO���������Ϊ20%)��H2O��Ӧ���õ�1.18 mol CO��CO2��H2�Ļ�����壬��CO��ת����Ϊ____________��
(3)��ͼ��ʾ500 �桢60.0 MPa�����£�ԭ����Ͷ�ϱ���ƽ��ʱNH3��������Ĺ�ϵ������ͼ��a�����ݼ���N2��ƽ�����������______________��
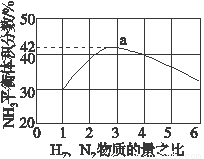
(4)��������ͼ�У�ʹ�ϳɰ��ų��������õ�������õ���Ҫ������(�����)_____________����������������ߺϳɰ�ԭ����ת���ʵķ�����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ӦX+Y�TM+NΪ���ȷ�Ӧ���Ը÷�Ӧ��˵����ȷ��( )
A��X������һ������M
B��Y������һ������N
C��X��Y��������һ������M��N��������
D����Ϊ�÷�ӦΪ���ȷ�Ӧ���ʲ��ؼ��ȾͿɷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶����¿�һ��ѧ�Ծ��������棩 ���ͣ�ʵ����
ijѧ��ͨ���ⶨ��Ӧ���������ų��������������к��ȡ�����50mL0.5mol/L��������50mL0.55mol/L��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ����ش��������⣺
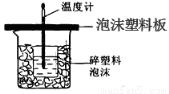
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��_____________����ͼ��֪��װ���в���֮���� ��
��2��ʵ���и���60 mL0.50 mol/L�������50mL 0.55 mol/L��NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������________�����ȡ����� �ȡ����������к��ȵ���ֵ��______________�����ȡ��� ������ȡ�����
�ȡ����������к��ȵ���ֵ��______________�����ȡ��� ������ȡ�����
��3����ͬѧ��ʵ��ʱ��Щ�������淶����ɲ���к��ȵ��� ֵƫ�ͣ�����������ܵ�ԭ��
ֵƫ�ͣ�����������ܵ�ԭ�� ��
��
A������������¶Ⱥ��¶ȼ�û����ˮ��ϴ�ɾ�
B������Ͳ�е�����������Һ����С�ձ�ʱ�����ٻ�
C������ʵ��ĵ������½ϸ�
D������ȡ����ʱ���Ӽ���
E����50mL0.55mol/L����������Һȡ����50mL0.55mol/L�İ�ˮ
��4����V1ml 1.0mol/L HCl��Һ��V2mlδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼�¶ȣ�ʵ��������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2=50mL��

ͨ������ͼ���֪������ʵ��ʱ�����¶� ������ڡ��������ڡ����ڡ���22�棬��NaOH��Һ��Ũ��ԼΪ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶����¿�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ͬ��ͬѹ�£����и����Ȼ�ѧ����ʽ�У���H1����H2��
A��C��s����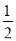 O2��g����CO��g������H1 C��s����O2��g����CO2��g������H2
O2��g����CO��g������H1 C��s����O2��g����CO2��g������H2
B��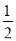 H2��g����
H2��g����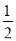 Cl2��g����HCl��g������H1 H2��g����Cl2��g����2HCl��g������H2
Cl2��g����HCl��g������H1 H2��g����Cl2��g����2HCl��g������H2
C��2H2��g����O2��g����2H2O��g������H1 2H2��g����O2��g����2H2O��l������H2
D��S��g����O2��g����SO2��g������H1 S��s����O2��g����SO2��g������H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶����¿�һ��ѧ���������棩 ���ͣ�������
����������ȼ�գ������������ֹ�̬�����6.2 g�ĵ����ף�P����6.4 g������ȼ�գ�����Ӧ��ľ������ų�a kJ������
��1 ��ͨ������ȷ����Ӧ�������ɣ��û�ѧʽ��ʾ���� ������Ӧ��������g��Ϊ ��
��ͨ������ȷ����Ӧ�������ɣ��û�ѧʽ��ʾ���� ������Ӧ��������g��Ϊ ��
��2����֪������ȼ����Ϊb kJ/mol����1mol P��O2��Ӧ���ɹ�̬P2O3�ķ�Ӧ�Ȧ�H�� ��
��3��д��1mol P��O2��Ӧ���ɹ�̬P2O3���Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
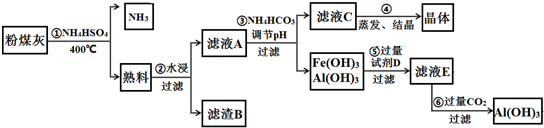
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ��ѧ��Ӧ�����ӷ���ʽ | ���� |
| A | AlCl3��Һ�м��������ˮ�� Al3++3NH3•H2O�TAl��OH��3��+3NH4+ | ������Ԫ�صIJ���Ӧ����AlO2- |
| B | ��������ͨ���廯������Һ�У� 3Cl2+2Fe2++4Br-�T6Cl-+2Fe3++2Br2 | ��ȷ |
| C | �ð�ˮ���չ����������� 2NH3•H2O+SO2�T2NH4++SO32-ʮH2O | ��ȷ |
| D | �Ȼ������ˮ�� NH4++2H2O�TH3O++NH3•H2O | �����Ȼ���ܽ���ˮ�������仯������д���ӷ���ʽ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com