
| A. | 30 | B. | 44 | C. | 46 | D. | 80 |
分析 n(Mg)=$\frac{0.96g}{24g/mol}$=0.04mol,n(HNO3)=$\frac{6.3g}{63g/mol}$=0.1mol,生成硝酸镁消耗n(HNO3)=2n(Mg)=2×0.04mol=0.08mol,剩余的0.02mol硝酸参加氧化还原反应,根据转移电子相等计算产物成分及其相对分子质量.
解答 解:n(Mg)=$\frac{0.96g}{24g/mol}$=0.04mol,n(HNO3)=$\frac{6.3g}{63g/mol}$=0.1mol,生成硝酸镁消耗n(HNO3)=2n(Mg)=2×0.04mol=0.08mol,剩余的0.02mol硝酸参加氧化还原反应,设生成物中N元素化合价为x,根据转移电子相等得0.04mol×2=0.02mol×(5-x),
x=+1,所以其产物可能是N2O也可能是NH4NO3,所以其相对分子质量可能是44也可能是80,故选BD.
点评 本题考查氧化还原反应的计算,为高频考点,根据转移电子相等计算其产物中N元素平均化合价即可,注意:硝酸铵中N元素平均化合价也是+1,为易错点.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
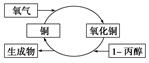
| A. | 1丙醇发生了还原反应 | |
| B. | 生成物可以发生银镜反应 | |
| C. | 反应中有红黑颜色交替变化的现象 | |
| D. | 2丙醇也能发生图示的催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
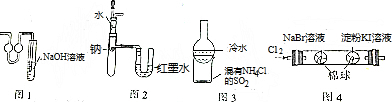
| A. | 图1装置用于二氧化硫尾气的吸收 | |
| B. | 图2装置用于验证Na和水反应的热效应 | |
| C. | 加热图3装置中的烧杯,分离SiO2和NH4Cl | |
| D. | 图4装置用于证明氧化性:Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第三次月考化学卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的是
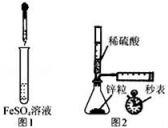
A.制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡
B.测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间
C.除去苯中少量苯酚:向苯和苯酚的混合液中加入浓溴水,过滤
D.检验淀粉是否水【解析】
取0.5 g淀粉于洁净的试管中,先加入5 mL稀硫酸,水浴加热,一段时间后再加入少量新制氢氧化铜悬浊液,水浴加热,观察实验现象
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:选择题
常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液 的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
A.两溶液混合,AgCl和AgI都沉淀
B.若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主
C.向AgI清液加入AgNO3,c(Ag+)增大,KSp(AgI)也增大
D.若 取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
在一恒容的密闭容器中充入2mol A和1mol B,发生反应2A(g)+B(g) xC(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6mol,B为0.3mol,C为1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为 ( )
xC(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6mol,B为0.3mol,C为1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为 ( )
A.只能为2 B.只能为3 C.可能是2,也可能是3 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com