
具有下列电子排布式的原子中,原子半径最大的是()
A. 1s22s22p63s23p2 B. 1s22s22p63s2
C. 1s22s22p2 D. 1s22s22p63s23p4
考点: 原子核外电子排布;微粒半径大小的比较.
专题: 原子组成与结构专题.
分析: 原子的电子层数越多,其原子半径越大,相同电子层数的原子,原子半径随着原子序数的增大而减小,据此分析解答.
解答: 解:原子的电子层数越多,其原子半径越大,相同电子层数的原子,原子半径随着原子序数的增大而减小,
根据原子核外电子排布式知,A、B和D电子层数都是3,C电子层数是2,所以A、B和D的原子半径大于C,
B的原子序数小于A和D,同一周期元素,原子半径随着原子序数的增大而减小,所以B的原子半径大于A和D,则原子半径最大的是B,
故选B.
点评: 本题考查了原子半径大小的判断,明确原子半径与电子层数、原子序数(相同电子层数)之间的关系即可解答,难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
(1)18O2﹣离子结构示意图 ,质量相等的O3和O2中,原子个数之比为 ;
(2)某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则该硫原子的相对原子质量为 ,m g该硫原子的物质的量为 mol;
(3)19g 某二价金属的氯化物ACl2 中含有0.4molCl﹣,ACl2的摩尔质量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
|
| A. |
实验室用乙醇制取乙烯 | B. |
实验室制取乙酸乙酯 |
|
| C. |
石油分馏 | D. |
实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
结构的研究是有机化学最重要的研究领域,某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式如下:(其中Ⅰ、Ⅱ为未知部分的结构).
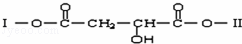
为推测X的分子结构,进行如下图转化:
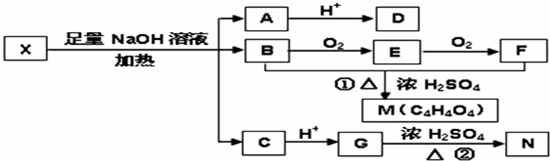
已知向D的水溶液中滴入FeCl3溶液显紫色,对D的结构进行光谱分析,在氢核磁共振谱上显示只有两种信号.M、N互为同分异构体,M中含有一个六原子环,N能使溴的四氯化碳溶液褪色,G能与NaHCO3溶液反应.请回答:
(1)D不可以发生的反应有(选填序号) ;
①加成反应 ②消去反应 ③氧化反应 ④取代反应
(2)写出上图转化中生成 M 的化学方程式:
(3)已知向X中加入FeCl3溶液,能发生显色反应,写出X的一种结构简式:_ 或
1mol该 X与足量的NaOH溶液作用,最多可消耗NaOH mol.
(4)有一种化工产品的中间体W与G互为同分异构体,W的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基.写出W的可能结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E代表5种元素.请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为N,其气态氢化物化学式为 .
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为 ,其最高价氧化物的水化物的化学式为 ,C的元素符号为K,C在周期表中的位置为 .
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为Fe,其基态原子的电子排布式为 .
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ,其基态原子的电子排布式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学用Na2CO3配制0.10mol/L Na2CO3溶液的过程如图所示.你认为该同学的错误有()

A. ①⑤⑥ B. ②④⑦ C. ①⑥ D. ⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
某待测液中只可能含有Ag+、Fe2+、Fe3+、Na+、Ba2+、CO32﹣、NO3﹣、SO42﹣中的几种离子,依次进行如下实验:
①取少量待测液,加入足量的NaCl溶液,无明显现象.
②继续加入足量的Na2SO4溶液,有白色沉淀生成.
③过滤,取少量滤液,加入足量NaOH溶液,有白色絮状沉淀生成,迅速变成灰绿色,最终变成红褐色.
根据实验现象回答:
(1)待测液中一定含有离子 ,一定没有离子 .
写出步骤②中发生反应的离子方程式 ,写出步骤③中沉淀由白色变为红褐色的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com