
【题目】有机制药工业中常用以下方法合成一种药物中间体(G):


(1)G的分子式是___。
(2)化合物A中含氧官能团的名称为___。
(3)由C→D的反应类型为___;化合物E的结构简式为___。
(4)写出B→C的反应的化学方程式:___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应;
②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9;
③分子中含有氨基。
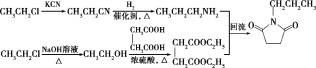
(6)已知:RCN![]() RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备
RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备![]() 的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH![]() CH2
CH2![]() CH2
CH2![]() CH3CH2Cl
CH3CH2Cl
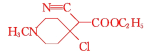
【答案】C11H18O2N2 羰基 取代反应 ![]()
![]() +HCl
+HCl![]()
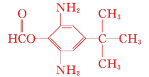 或
或
【解析】
⑴根据G的结构式数出G的分子式。
⑵化合物A中含氧官能团的名称为羰基。
⑶对比C、D的结构简式可知C→D反应类型,E与乙醇发生酯化反应得到F,由F的结构简式逆推得,E的结构简式。
⑷对比B、C的结构简式可知,B中碳碳双键与HCl发生加成反应生成C。
⑸根据同时满足条件的书写B的同分异构体。
⑹由F→G的转化可知,CH3CH2CH2NH2与CH3CH2OOCCH2CH2COOCH2CH3反应得到 ,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3。
,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3。
⑴根据G的结构式数出G的分子式是C11H18O2N2,故答案为:C11H18O2N2。
⑵化合物A中含氧官能团的名称为羰基,故答案为:羰基。
⑶对比C、D的结构简式可知,C中的—Cl被—CN取代生成D,所以C→D属于取代反应;由题图知,E与乙醇发生酯化反应得到F,由F的结构简式逆推得,E的结构简式为![]() ,故答案为:取代反应;
,故答案为:取代反应;![]() 。
。
⑷对比B、C的结构简式可知,B中碳碳双键与HCl发生加成反应生成C,B→C的反应的化学方程式为![]() +HCl
+HCl![]()
![]() ,故答案为:
,故答案为:![]() +HCl
+HCl![]()
![]() 。
。
⑸同时满足下列条件的B的同分异构体:①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应,说明含有甲酸与酚形成的酚酯基,即取代基为—OOCH,③分子中含有氨基,②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9,存在对称结构,还含有2个—NH2、1个—C(CH3)3,符合条件的B的同分异构体为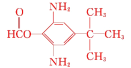 或
或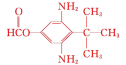 ,故答案为:
,故答案为: 或
或 。
。
⑹由F→G的转化可知,CH3CH2CH2NH2与CH3CH2OOCCH2CH2COOCH2CH3反应得到 ,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3,故答案为:
,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3,故答案为:
 。
。


科目:高中化学 来源: 题型:
【题目】已知某饱和溶液中:①溶液的质量;②溶剂的质量;③溶液的体积;④溶质的摩尔质量;⑤溶质的溶解度;⑥溶液的密度,从上述条件中不能用来计算该饱和溶液的物质的量浓度的是( )
A.④⑤⑥B.①②③④C.①②④⑥D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种有机化合物的键线式如图所示。下列说法错误的是
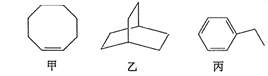
A. 甲、乙的化学式均为C8H14
B. 乙的二氯代物共有7种(不考虑立体异构)
C. 丙的名称为乙苯,其分子中所有碳原子可能共平面
D. 甲、乙、丙均能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如图:

已知:R1CH2COOCH2CH3+R2COOCH2CH3![]()
![]() +CH3CH2OH
+CH3CH2OH
(1)化合物A的名称是_____。
(2)反应②和⑤的反应类型分别是_____、_____。
(3)写出C到D的反应方程式_____。
(4)E的分子式_____。
(5)F中官能团的名称是_____。
(6)X是G的同分异构体,X具有五元碳环结构,其核磁共振氢谱显示四组峰,且峰面积之比为6:2:1:1。写出两种符合要求的X的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列表示物质变化的化学用语中正确的是( )
A. 汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-=PbSO4+4H++SO42-
B. 利用Na2CO3溶液可除油污:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. BaSO4的水溶液导电性极弱: BaSO4![]() Ba2++SO42-
Ba2++SO42-
D. 用醋酸除去暖瓶中的水垢:2H++ CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对拟卤素的性质进行探究,设计了以下实验( )
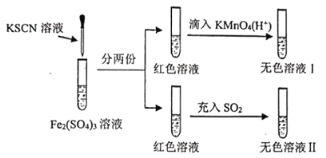
已知:(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是( )
A.溶液颜色变红时发生反应的离子方程式是:Fe3++3SCN-=Fe(SCN)3↓
B.红色溶液褪色表现了的漂白性
C.氧化性:KMnO4>Fe3+>(SCN)2
D.无色溶液Ⅱ中滴入适量的KMnO4(H+)溶液,溶液又变成红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KIO3与H2S反应制备KI固体,装置如图所示。实验步骤:①检查装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得KIO3;③打开K,通入H2S直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加热,充分逸出H2S;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可得成品。下列有关该实验的叙述错误的是( )
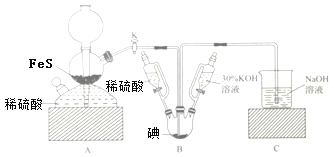
A.步骤②可观察到固体溶解,溶液由棕黄色变为无色
B.步骤③装置B中发生反应的离子方程式为3H2S+IO3-═3S↓+3H2O+I-
C.装置C中氢氧化钠溶液的作用是吸收硫化氢
D.步骤⑤中一系列操作为过滤,洗涤,合并滤液和洗液,蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是( )
A.0.1mol/L的FeCl3溶液与0.01mol/L的FeCl3溶液中,Fe3+的浓度之比大于10
B.将a mol·L-1的氨水与0.01mol·L-1的盐酸等体积混合后,c(NH4+)=c(Cl-),则NH3·H2O的电离常数为![]()
C.pH加和为12的强酸与弱酸混合,pH可能为6
D.0.1mol·L-1 NH4HS溶液中有:c(NH4+)=c(HS-)+c(S2-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,可通过实验的方法加以确定,下列说法中错误的是( )
A. 加入含有NaOH的酚酞溶液,红色褪去,说明有H+存在
B. 加入有色布条后,有色布条退色,说明有HClO分子存在
C. 氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
D. 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com