
| A、HT、D2互为同素异形体 |
B、HF的电子式: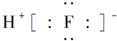 |
C、NH4Cl的电子式: |
D、CaC2的电子式: |
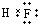 ,故B错误;
,故B错误;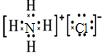 ,故C错误;
,故C错误; ,故D正确;
,故D正确;

科目:高中化学 来源: 题型:
| A、溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | ||
B、乙醇与溴水溶液反应:C2H5OH+HBr
| ||
C、甲苯与浓硝酸和浓硫酸的混合物反应: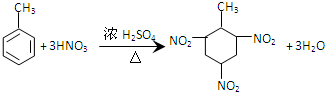 | ||
D、实验室用液溴和苯制溴苯: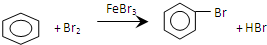 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(CH3)2CHCH2CH2CH3 |
| B、(CH3CH2)2CHCH3 |
| C、(CH3)2CHCH(CH3)2 |
| D、(CH3)3CCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、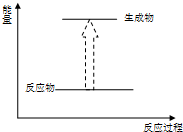 化石燃料的燃烧 |
B、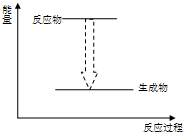 植物的光合作用 |
C、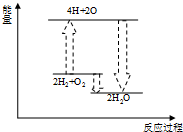 氢气与氧气反应 |
D、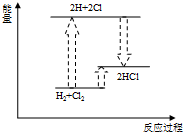 氢气与氯气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑤ | B、①②⑤⑦ |
| C、②⑤⑥ | D、①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl溶液与苏打溶液混合:2NH4++CO32-═2NH3↑+CO2↑+H2O | ||||
| B、向Mg(OH)2沉淀中加入FeCl3溶液:3Mg(OH)2+2Fe3+═3Mg2++2Fe(OH)3 | ||||
C、用石墨作电极电解AlCl3溶液:2Cl-+2H2O
| ||||
| D、FeCl3溶液与Na2SO3溶液混合:2Fe3++3SO32-+3H2O═2Fe(OH)3↓+3SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、可与NaOH和NaHCO3发生反应 |
| B、1mol该有机物可以与7mol H2发生反应 |
| C、可以用有机溶剂萃取 |
| D、1mol该有机物可以与5mol Br2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 导管及仪器 |  |
 |
 |
 |
 |
 |
| 每个橡皮塞上都打了两个孔 | ||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com