
取一定量![]() 、
、![]() 和
和![]() 的混合物与
的混合物与![]()
![]() 过量的盐酸反应,生成标准状况下
过量的盐酸反应,生成标准状况下![]() 的气体,然后加入
的气体,然后加入![]()
![]()
![]() 溶液,得到沉淀质量
溶液,得到沉淀质量![]() ,溶液中过量的碱用
,溶液中过量的碱用![]()
![]() 盐酸恰好完全中和,计算原混合物中各物质的质量。
盐酸恰好完全中和,计算原混合物中各物质的质量。
科目:高中化学 来源: 题型:
Ⅰ.实验表明,CuO被H2还原时也有Cu2O生成。将一定量的H2缓慢通过灼热的CuO粉末,得到固体混合物且混合物中m(Cu)∶m(O)=8∶a。当a有不同的取值时,固体混合物成分不同。请分析a的取值范围和固体混合物成分的关系并填入下表(不一定填满,表格不够也可自行增加)。
a的取值范围 | 反应后固体的成分(用化学式表示) |
|
|
|
|
|
|
Ⅱ.黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀释至2.12 L时测得其pH为0;将稀释后的溶液分为两等份,向其中一份溶液中滴加6.05 mol·L-1的NaOH溶液,向另一份溶液中滴加0.600 mol·L-1 Ba(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
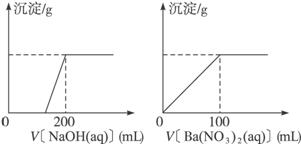
(1)请通过计算确定m的值;
(2)X的摩尔质量为368 g·mol-1,请确定X的化学式_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.实验表明,CuO被H2还原时也有Cu2O生成。将一定量的H2缓慢通过灼热的CuO粉末,得到固体混合物且混合物中m(Cu)∶m(O)=8∶a。当a有不同的取值时,固体混合物成分不同。请分析a的取值范围和固体混合物成分的关系并填入下表(不一定填满,表格不够也可自行增加):
a的取值范围 | 反应后固体的成分(用化学式表示) |
|
|
|
|
|
|
Ⅱ.黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀释至2.12 L时测得其pH为0;将稀释后的溶液分为两等份,向其中一份溶液中滴加6.05 mol·L-1的NaOH溶液,向另一份溶液中滴加0.600 mol·L-1 Ba(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
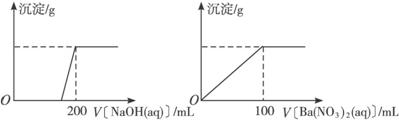
(1)请通过计算确定m值。
(2)X的摩尔质量为368 g·mol-1,请确定X的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳和铝是常见的还原剂。
(1)碳与铝分别在氧气中燃烧,产生非极性分子A与固体B,A的分子式是 。
(2)用NaOH溶液把(1)中的B刚好溶解后得到溶液C,然后把少量A通到C溶液中,反应后过滤可得Al(OH)3沉淀和滤液。则下列说法正确的是 (填序号)。
a.A溶于水后促进了NaAlO2的水解,产生Al(OH)3沉淀
b.A l(OH)3(胶体)能凝聚水中悬浮物,可用来净水
c.若取滤液少量,在火焰上灼烧,火焰的颜色为黄色
d.若向滤液中滴加足量硝酸酸化的AgNO3溶液,最后有沉淀产生
(3)若向溶液C中滴入Al2(SO4)3溶液也会得到Al(OH)3沉淀。该反应的离子方程式是 。
(4)碳、铝均能还原铁的氧化物。为确定混合物(FeO、Fe2O3)的组成,进行如下实验:
①取一定量混合物与足量碳粉加热,只收集到CO气体m mol;
②取与①相同量的混合物与足量铝进行铝热反应,得到单质铁n mol;
则混合物中FeO的物质的量分数是 ;②中铝的物质的量至少 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)取一定量的Na2CO3、NaHCO3和![]() 的混合物与250ml,100mo1?L-1过量盐酸反应,生成2016LCO2(标准状况),然后加入500ml,0100mo1L-1Ba(OH)2溶液,得到沉淀的质量为233g,溶液中过量的碱用100ml,100mo1?L-1盐酸恰好完全中和。计算混合物中各物质的质量。
的混合物与250ml,100mo1?L-1过量盐酸反应,生成2016LCO2(标准状况),然后加入500ml,0100mo1L-1Ba(OH)2溶液,得到沉淀的质量为233g,溶液中过量的碱用100ml,100mo1?L-1盐酸恰好完全中和。计算混合物中各物质的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com