
| A. | 取a g混合物用酒精灯充分加热后质量减少b g | |
| B. | 取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收后质量增加b g | |
| C. | 取a g混合物与足量氢氧化钡溶液充分反应,过滤、洗涤、烘干,得b g固体 | |
| D. | 取a g混合物于锥形瓶中加水溶解,滴入1~2滴酚酞指示剂,用标准盐酸溶液滴定至终点,消耗盐酸V mL |
分析 A.Na2CO3较稳定,受热不易分解,NaHCO3不稳定,受热易分解;
B.碱石灰也能吸收水蒸气;
C.根据质量关系,可列方程组求解;
D.根据VmL盐酸可知道盐酸的物质的量,根据二者的质量和消耗盐酸的物质的量,可计算出Na2CO3质量分数.
解答 解:A.NaHCO3受热易分解生成碳酸钠、水和二氧化碳,通过加热分解利用差量法即可计算出Na2CO3质量分数,故A不选;
B.混合物与足量稀硫酸充分反应,也会生成水和二氧化,所以逸出的气体是二氧化碳,但会混有水蒸气,即碱石灰增加的质量不全是二氧化碳的质量,不能测定含量,故B选;
C.Na2CO3和NaHCO3都与Ba(OH)2反应,反应的方程式为CO32-+Ba2+=BaCO3↓、HCO3-+OH-+Ba2+=H2O+BaCO3↓,因此最后得到的固体是BaCO3,所以可以计算出Na2CO3质量分数,故C不选;
D.Na2CO3和NaHCO3均可与盐酸反应生成水、二氧化碳和氯化钠,所以根据VmL盐酸可知道盐酸的物质的量,根据二者的质量和消耗盐酸的物质的量,可计算出Na2CO3质量分数,故D不选;
故选B.
点评 本题考查化学实验方案评价,为高频考点,侧重考查学生分析判断及计算能力,明确实验原理、物质性质及其差异性是解本题关键,注意B中干燥剂不仅吸收二氧化碳还吸收水蒸气,注意隐含信息的挖掘,易错选项是B.


科目:高中化学 来源: 题型:多选题
| A. | 银锌纽扣电池工作时,Ag2O被还原为Ag | |
| B. | 碱性锌锰电池中,MnO2是催化剂 | |
| C. | 放电时,铅酸蓄电池中硫酸浓度不断增大 | |
| D. | 电镀时,待镀的金属制品表面发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
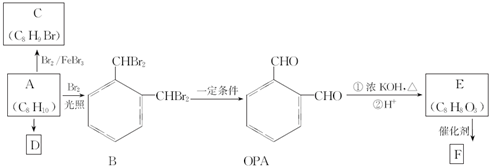
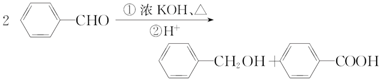
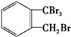 .
.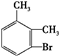 、
、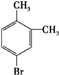 .
.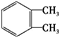 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$ $→_{△}^{CH_{3}CH_{2}OH、浓硫酸}$
$→_{△}^{CH_{3}CH_{2}OH、浓硫酸}$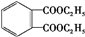 .
.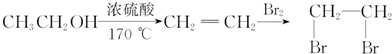
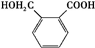 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$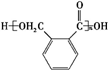 +(n-1)H2O.
+(n-1)H2O.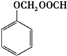 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
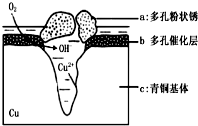 青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )| A. | 腐蚀过程中,负极 b 被氧化 | |
| B. | 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ | |
| C. | 若生成 2.145gCu 2 ( OH ) 3 Cl,则理论上消耗标准状况氧气体积为 0.448L | |
| D. | 正极的电极反应式为:正极反应是 O2+4e-+2H2O=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
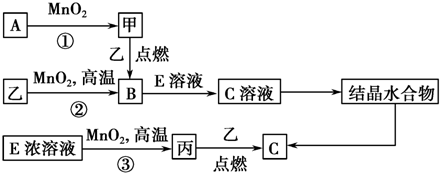
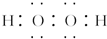 .若反应①需在加热条件下进行,则反应①的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.
.若反应①需在加热条件下进行,则反应①的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )
在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )| A. | 该反应在0~t1时间段的速率为:ν(W)=0.25/t1 mol•L-1•min-1 | |
| B. | 反应方程式中的a不可能等于1 | |
| C. | t2时刻改变的条件是通入少量气体Z | |
| D. | t3时刻改变的条件是移去少量物质W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由上述热化学方程式可知d>c | |
| B. | H2的燃烧热为d kJ/mol | |
| C. | CH3OH(g)═CO(g)+2H2(g)△H=(b+2c-a)kJ/mol | |
| D. | 当CO和H2的物质的量之比为1:2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为$\frac{Q}{b+2c}$mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com