
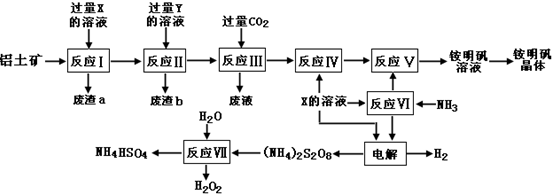
分析 铝土矿(主要成分为Al2O3和少量的 SiO2、Fe2O3杂质)铝土矿的主要成分是氧化铝,根据题中流程图可知,在反应Ⅲ中通入二氧化碳,而流程最后要得到硫酸盐,所以为了除去杂质,先在铝土矿中加入过量的稀硫酸,得废渣a为SiO2,滤液中含有Al3+、Fe3+,所以X为稀硫酸,再加过量的氢氧化钠溶液,生成偏铝酸钠溶液和氢氧化铁沉淀,所以废渣b为氢氧化铁,Y为氢氧化钠,反应Ⅲ为偏铝酸钠溶液与过量二氧化碳反应生成氢氧化铝沉淀和废液,反应Ⅳ为氢氧化铝中加上硫酸可以制得Al2(SO4)3,反应Ⅵ中氨气与硫酸反应生成(NH4)2SO4,反应Ⅴ中(NH4)2SO4转化为铵明矾,电解硫酸和硫酸铵的混合溶液,在阴极上得氢气,阳极上得(NH4)2S2O8,反应ⅤⅡ为(NH4)2S2O8与水反应生成双氧水和NH4HSO4,以此来解答.
解答 解:铝土矿(主要成分为Al2O3和少量的 SiO2、Fe2O3杂质)铝土矿的主要成分是氧化铝,根据题中流程图可知,在反应Ⅲ中通入二氧化碳,而流程最后要得到硫酸盐,所以为了除去杂质,先在铝土矿中加入过量的稀硫酸,得废渣a为SiO2,滤液中含有Al3+、Fe3+,所以X为稀硫酸,再加过量的氢氧化钠溶液,生成偏铝酸钠溶液和氢氧化铁沉淀,所以废渣b为氢氧化铁,Y为氢氧化钠,反应Ⅲ为偏铝酸钠溶液与过量二氧化碳反应生成氢氧化铝沉淀和废液,反应Ⅳ为氢氧化铝中加上硫酸可以制得Al2(SO4)3,反应Ⅵ中氨气与硫酸反应生成(NH4)2SO4,反应Ⅴ中(NH4)2SO4转化为铵明矾,电解硫酸和硫酸铵的混合溶液,在阴极上得氢气,阳极上得(NH4)2S2O8,反应ⅤⅡ为(NH4)2S2O8与水反应生成双氧水和NH4HSO4,
(1)由上述分析可知,废渣a为SiO2,名称为二氧化硅,废渣b为氢氧化铁,
故答案为:二氧化硅;氢氧化铁;
(2)根据上面的分析可知,流程图中X为稀硫酸,X的化学式为H2SO4,
故答案为:H2SO4;
(3)反应Ⅲ为偏铝酸钠溶液与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,反应Ⅲ的离子方程式为 AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓,铵明矾晶体中有结晶水,温度过高会使结晶水失去,所以从铵明矾溶液中获得铵明矾晶体的操作依次为 蒸发浓缩、冷却结晶、过滤、洗涤,
故答案为:AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓;蒸发浓缩;
(4)根据电解原理阳极失电子发生氧化反应,SO42?失电子生成S2O82-,电极方程式为2SO42--2e-═S2O82-,
故答案为:2SO42--2e-═S2O82-;
(5)根据元素守恒和题中信息可知,反应Ⅶ的化学方程式为(NH4)2S2O8+2H2O=2NH4HSO4+H2O2,NH4HSO4溶液中电离出SO42-、H+、NH4+,其中铵根离子水解生成氢离子,所以溶液中离子浓度由大到小顺序为c(H+)>c(SO42-)>c(NH4+)>c(OH-),
故答案为:(NH4)2S2O8+2H2O=2NH4HSO4+H2O2;c(H+)>c(SO42-)>c(NH4+)>c(OH-);
(6)设NH4Al(SO4)2为2mol,逐滴加入氢氧化钡溶液,则;
A.如Al3+完全转化为AlO2-,则需要5molBa(OH)2,此时发生2NH4Al(SO4)2+5Ba(OH)2=2NH3•H2O+4BaSO4↓+Ba(AlO2)2+4H2O,则n(NH4Al(SO4)2):n(Ba(OH)2)<2时,生成产物为(NH4)2SO4、BaSO4↓、Al(OH)3,可能含有Al2(SO4)3,故A不选;
B.n(NH4Al(SO4)2):n(Ba(OH)2)=2时,生成产物为NH3•H2O、BaSO4和Al(OH)3,故B选;
C.设NH4Al(SO4)2为2mol,溶液中含有2molNH4+、2molAl3+、4molSO42-,Al3+完全沉淀时,需要3molBa(OH)2,此时发生2NH4Al(SO4)2+3Ba(OH)2=(NH4)2SO4+3BaSO4↓+2Al(OH)3↓,故C不选;
D.如SO42-完全反应,则需要4molBa(OH)2,此时发生NH4Al(SO4)2+2Ba(OH)2=NH3•H2O+2BaSO4↓+Al(OH)3↓,故D不选;
故选B.
点评 本题考查制备实验方案的设计,为高频考点,侧重考查化学流程的分析、基本操作、电解原理、离子浓度比较、化学反应的判断,把握工艺流程及发生的反应、混合物分离提纯等为解答的关键,题目难度中等,需要学生具备阅读获取信息能力、综合运用知识、信息分析问题解决问题能力.


 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
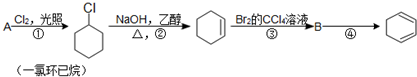
 ,名称是环己烷.
,名称是环己烷. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O═Ca(OH)2 | B. | 2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO | ||
| C. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | D. | Cu(OH)2 $\frac{\underline{\;△\;}}{\;}$CuO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2LSO2和2LCO2 | B. | 9 g水和标准状况下 11.2LCO2 | ||
| C. | 标准状况下1mol氧气和 22.4L水 | D. | 0.1mol氢气和 2.24L氯化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仍平衡 | B. | 盛钠的一端下沉 | C. | 盛镁的一端下沉 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl+NaOH$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O+NaCl | B. | 3CO+Fe2O3$\frac{\underline{\;△\;}}{\;}$2Fe+3CO2 | ||
| C. | Cl2+2KBr═Br2+2KCl | D. | NH3+CO2+H2O═NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
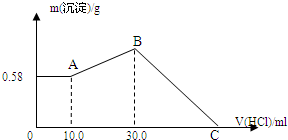 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生0.58g白色沉淀,再向所得悬浊液中逐滴加入0.5mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生0.58g白色沉淀,再向所得悬浊液中逐滴加入0.5mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com