
A.实验室制取乙烯的反应原理:C2H5OH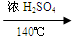 C2H4 ↑+ H2O C2H4 ↑+ H2O |
| B.实验室制取C2H2,一般用碳化钙跟饱和食盐水反应以适度减缓反应速率 |
| C.实验室分离苯和苯酚的混合物,可采用溴水 |
| D.由1—溴丁烷跟氢氧化钠醇溶液共热,可以制得两种烯烃 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
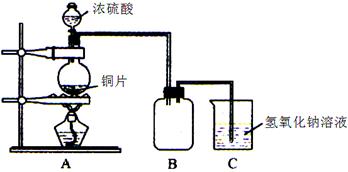
| 方案序号 | 分析 | 误差(偏低或偏高) | 改变措施 |
| | | | |
| | | | |
| | | | |
| | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
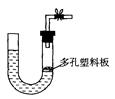
| A.大理石和稀硫酸制取二氧化碳 |
| B.锌粒和稀硫酸制氢气 |
| C.浓盐酸和二氧化锰制取氯气 |
| D.电石和水制取乙炔 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3固体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2、O2、HCl | B.O2、NO2、NO | C.O2、NH3、H2 | D.CO2、O2、NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
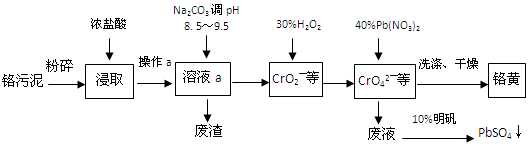
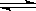 Al(OH)3 +3H+的平衡常数为 。
Al(OH)3 +3H+的平衡常数为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制备乙炔:实验室不能用启普发生器来制取乙炔 |
| B.制备乙酸乙酯:将乙醇和乙酸混合,再加入稀硫酸共热 |
| C.制备一氯乙烷:将乙烷和氯气的混合气放在光照条件下反应 |
| D.制备乙烯:实验室用无水乙醇和浓硫酸共热到170℃制取乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

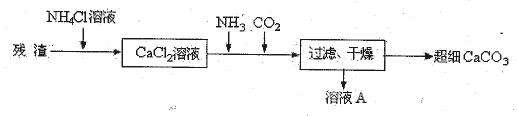
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com