

| ||
| ||


科目:高中化学 来源: 题型:
A、甲烷与氯气反应制氯仿:CH4+3Cl2
| ||
B、烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2
| ||
C、甲烷、CO合成乙酸乙酯:2CH4+2CO
| ||
D、乙烯合成聚乙烯nCH2-CH2
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、火山喷发产生的火山灰中不可能含有SO3气体 |
| B、等物质的量的SO2与Cl2同时通入水中,所得溶液的漂白性增强、pH减小 |
| C、BaSO3能够溶于稀盐酸,所以可以用Ba(NO3)2溶液、稀盐酸鉴别SO2和SO3 |
| D、一定条件下,铁粉与硫的最高价氧化物对应的水化物的溶液反应,可以得到两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molCl2与足量Fe反应,转移的电子数为3NA |
| B、0.1mol铁粉与足量的高温水蒸气作用,生成的H2分子数为0.1NA |
| C、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| D、1mol的Na2O2中阴离子个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
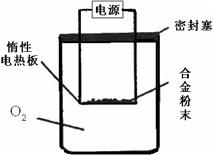 锌和铝都是活泼金属,化学性质相似,其氢氧化物既能溶于强酸,也能溶于强碱,都是两性氢氧化物.但是氢氧化铝不溶于氨水,而氢氧化锌却溶于氨水生成[Zn(NH3)4]2+,回答下列问题:
锌和铝都是活泼金属,化学性质相似,其氢氧化物既能溶于强酸,也能溶于强碱,都是两性氢氧化物.但是氢氧化铝不溶于氨水,而氢氧化锌却溶于氨水生成[Zn(NH3)4]2+,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用苯从溴水中提取溴,有机层从分液漏斗的上口倒出 |
| B、实验室可以用浓氨水和生石灰制备NH3 |
| C、实验室中用加热方法分离碘和食盐的混合物 |
| D、加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com