
【题目】有甲、乙两个装置,下列说法错误的是

甲 乙
A.甲、乙装置中,Zn的质量均减小
B.甲、乙装置中,Cu上均有气泡产生
C.化学反应速率:乙>甲
D.甲装置中H+移向Zn,乙装置中H+移向Cu
【答案】B
【解析】甲装置中的两种金属未用导线连接,所以不能构成原电池。乙装置符合原电池的构成条件,构成了原电池,锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,作原电池负极的金属腐蚀速率较快,原电池放电时,阳离子向正极移动。A项,甲、乙装置中锌都失去电子转化成锌离子进入溶液,所以锌的质量均减小,故A项正确。B项,甲装置中,锌和氢离子发生置换反应生成氢气,所以锌附近有气泡产生,乙装置构成原电池,氢离子在正极铜上得电子生成氢气,故B项错误。C项,甲装置不能构成原电池,乙装置能构成原电池,反应速率:乙>甲,故C项正确。D项,甲装置中氢离子在锌附近得电子发生还原反应,乙装置中氢离子在铜上得电子发生还原反应,所以甲装置中H+移向Zn,乙装置中H+移向Cu,故D项正确。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为硫的价类图,例如d点可表示+6价的硫酸盐.下列说法错误的是( ) 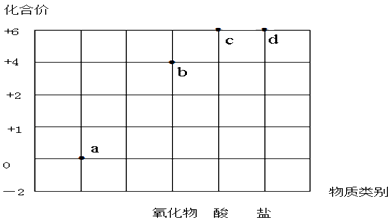
A.a点表示的物质所属的物质类别是单质
B.b点表示的物质可以是SO2或SO3
C.c点表示的化合物的浓溶液可作为干燥剂
D.d点表示的可溶性物质能与BaCl2溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁加热至高温会分解,生成—种金属氧化物M和两种非金属氧化物。某化学研究小组利用下列装置加热至高温使FeSO4分解。
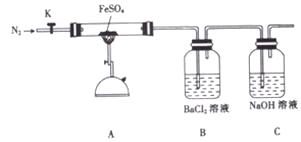
实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为_____________。
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
操作步骤 | 实验现象 | 用方程式解释原因 |
打开K,通入一段时间N2,关闭K。加热A中玻璃管一段时间 | 洗气瓶B中①__________ | ②______________ |
A中固体不再分解后,停止加热,打开K,缓慢通入N2至玻璃管冷却 | 硬质玻璃管最终可以看到③_______________ | ④______________ |
(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N。
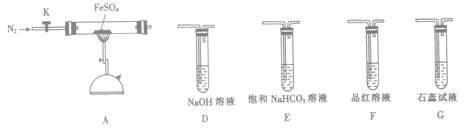
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→______→______。
②能证明生成了非金属氧化物N的现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称________,可作为碱使用的原因是___________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1
②NaOH(s)+CO2(g)= NaHCO3(s) ΔH1=131.5 kJ·mol1
反应2NaHCO3 (s)= Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=_______ kJ·mol1,该反应的平衡常数表达式K=________。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中![]() =_____________(保留三位有效数字)。已知Ksp(BaCO3)=2.6×109,Ksp(BaSO4)=1.1×1010。
=_____________(保留三位有效数字)。已知Ksp(BaCO3)=2.6×109,Ksp(BaSO4)=1.1×1010。
(4)已知室温时,Ksp[Mg(OH)2]=4.0×1011。在0.1 mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是_____________(已知lg2=0.3) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式,正确的是( )
A. 甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
C. HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
D. 500 ℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,合理的是( )。

A. 图①:验证H2CO3酸性强于H2SiO3 B. 图②:收集CO2或NH3
C. 图③:分离Na2CO3溶液与CH3COOC2H5 D. 图④:分离C2H5OH与CH3COOC2H5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com