
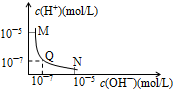 25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH-)的变化关系如图所示,则( )
25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH-)的变化关系如图所示,则( )

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
 CO(g)+H2(g)△H=+131kJ?mol-1
CO(g)+H2(g)△H=+131kJ?mol-1| 容器 编号 |
c(H2O) /mol?L-1 |
c(CO) /mol?L-1 |
c(H2) /mol?L-1 |
v正、v逆比较 |
| I | 0.06 | 0.60 | 0.10 | v正=v逆 |
| II | 0.06 | 0.50 | 0.40 | ① |
| III | 0.12 | 0.40 | 0.80 | v正<v逆 |
| IV | 0.12 | 0.30 | ② | v正=v逆 |
 CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)
CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示) 2Cu+CO2
2Cu+CO2 2Cu+CO2
2Cu+CO2查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(PH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/ml | 26.02 | 25.35 | 25.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、101 kPa时,1 mol H2燃烧生成水蒸气放出的热量叫做H2的燃烧热 | B、0.25molNa2O2中含有的阴离子数约为0.25×6.02×1023 | C、向0.2 mol?L-1NaHCO3溶液中加入等体积0.1 mol?L-1NaOH溶液,反应后溶液中:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | D、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市杨浦区高三上学期期末学业质量调研化学试卷(解析版) 题型:选择题
25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH—)的变化关系如图所示,则
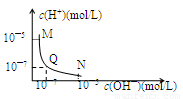
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO―)>c(Na+)
C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
D.M点和N点所示溶液中H2O的电离程度相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com