
下列文字表述与反应方程式对应且正确的是
A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O
B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:
HCO3-+ Ba2++OH- = BaCO3↓ + H2O
C. NaHSO3溶液显酸性的原因是:HSO3- = SO32- + H+
D. 硫化钠水溶液呈碱性的原因是:S2- + 2H2O  H2S + 2OH-
H2S + 2OH-
科目:高中化学 来源: 题型:
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,下列关于X、Y、Z、W四种元素的描述,不正确的是
A. 离子半径:X+>Y2+>W2->Z- B.原子半径:X>Y>W>Z
C.原子序数:Y>X>Z>W D.原子最外层电子数:Z>W>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)= 1.8×10-10,Ksp(AgY)= 1.0×10-12,Ksp(AgZ)= 8.7×10-17;
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-) (填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中c(Y-)= mol/L
(4)①由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
② 在上述(3)的体系中,能否实现AgY向AgX的转化?
请通过计算,简述能否实现转化的理由是:
查看答案和解析>>
科目:高中化学 来源: 题型:
将钠、镁、铝各0.3 mol,分别放入100 mL 1 mol·L—1的硫酸中,同温同压下产生的气体的体积比是( )
A.1∶2∶3 B.6∶3∶2 C.3∶2∶2 D.3∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生为探究钠与CO2的反应,利用如下装置进行实验。(已知PdCl2能被CO还原得到黑色的Pd)。可供选择的药品有:CaCO3(块状)、Na2CO3(粉末)、盐酸、稀硫酸、钠。
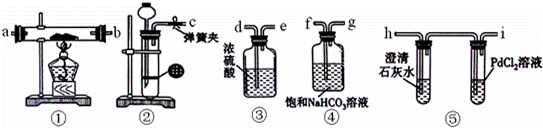
(1)请将上图各装置连接完整:②→ → →①→ 。(填装置序号)
(2)装置②有孔塑料板上所放的药品是: 。
(3)检查装置气密性并装好药品后,当观察到 现象时才点燃酒精灯,此步骤操作的目的是 。
(4)已知CO在潮湿环境中可将PdCl2还原为黑色粉末状的钯(Pd),写出该反应的化学方程式 。
(5)实验过程中CO2足量,装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。据此现象写出Na与CO2反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。
(1)写出该实验制备纯碱的反应方程式 、 。
(2)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是
(填字母标号)。a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
d.碳酸氢钠的稳定性大于碳酸钠
(3)某活动小组根据上述制碱原理,进行碳酸氢钠的制备实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验
装置如下图所示(图中夹持、固定用的仪器未画出)。试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 ,其作用是 ;
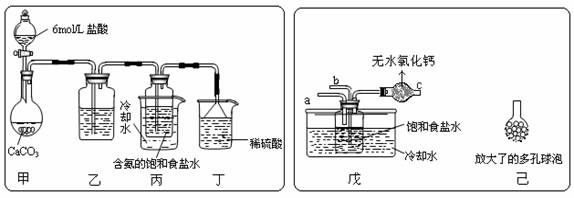 (Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称),该操作所需要的玻璃仪器有
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从a管通入_______气体,说明原因_________________________
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
(4) 碳酸氢钠受热所得固体12.28g与足量的石灰水充分反应,所得沉淀经洗
涤、干燥质量为12.00g,则所得固体中碳酸钠的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式
N2 + 3H2 = 2NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
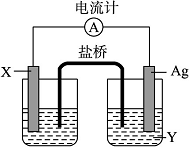 (1)电极X的材料是______;电解质溶液Y是______;
(1)电极X的材料是______;电解质溶液Y是______;
(2)银电极为电池的______极,发生的电极反应为______________;X电极上发生的电极反应为________________________________________;
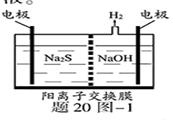
(3)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。(1)将烧碱吸收H2S后的溶液加入到如题20图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e- S
S
(n—1)S+ S2- Sn2-
Sn2-
①写出电解时阴极的电极反应式:_________________________
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
__________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气,或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是( )
A.(Ⅰ)用① B.(Ⅱ)用② C.(Ⅲ)用③ D. (Ⅳ)用④
(Ⅳ)用④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com