
【题目】回答下列问题:

(1)当电极a为A1、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:_____________。
(2)当电极a为Fe、电极b为Cu、电解质溶液为浓硝酸时,该装置_______(填“能”或“不能”)形成原电池,若不能,请说明理由________________________;若能,请写出该电池负极的电极反应方程式____________________。
(3)设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液为电解液;则CH4应通入_______极(填a或b,下同),电子从_______极流出。电池的负极反应方程式为____________。
【答案】2H++2e-=H2↑ 能 Cu-2e-=Cu2+ b b CH4+2H2O-8e-=CO2+8H+
【解析】
(1)Al、Cu、稀硫酸构成的原电池,金属铝做负极,金属铜为正极,正极上氢离子得电子生成氢气;
(2)自发的氧化还原反应能设计成原电池,失电子的极是负极;
(3)燃料电池中,甲烷燃料在负极通入,正极是氧气得电子,电子从负极流向正极。
(1)Al、Cu、稀硫酸构成的原电池,金属铝做负极,金属铜为正极,正极上氢离子得电子生成氢气,正极的电极反应为2H++2e-=H2↑;
(2)Fe、Cu、浓硝酸之间,金属Fe遇到浓硝酸会钝化,Cu与浓硝酸反应,则能设计成原电池,失电子的是金属铜,为负极,金属铁为正极,负极反应式为Cu-2e-=Cu2+;
(3)氢氧燃料电池中,燃料甲烷需通在负极,即CH4应通入b极,正极是氧气得电子,电子从负极流向正极,即电子从b极流出。负极上甲烷失电子生成二氧化碳,则负极电极反应方程式为CH4+2H2O-8e-=CO2+8H+。


科目:高中化学 来源: 题型:
【题目】(1)煤的气化是将其转化为可燃性气体的过程,主要化学反应方程式为__________。煤也可以直接液化,属于________________(填“化学变化”或“物理变化”)。
(2)由乙烯合成聚乙烯的化学方程式为_______________该高分子化合物的链节为___;若该高分子化合物的相对分子质量为42 000,则其聚合度为__。
(3)一种甲烷水合物晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,这种可燃冰的平均组成可表示为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是______________________________。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________(填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________。
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________极,阴极的电极反应式是____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式BaCO3+2H+═CO2↑+H2O+Ba2+中的H+不能代表的物质( ) ①H2SO4②NaHSO4③HNO3④HCl ⑤CH3COOH.
A.①②⑤
B.①④⑤
C.②④⑤
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(2)298 K时,在2L的密闭容器中,发生可逆反应:
2NO2(g)![]() N2O4(g) ΔH=-a kJ·mol-1(a>0)
N2O4(g) ΔH=-a kJ·mol-1(a>0)
N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。

①298k时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
试分析图中a、b、c、d、e五个点,
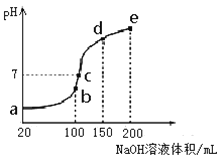
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组粒子,属于同种核素的是___________(填编号,下同),互为同位素的是___________,互为同素异形体的是___________,互为同分异构体的是___________,属于同种物质的是_____________,互为同系物的是_________。
①16O2和18O3 ②CH4和C3H8 ③![]() 、D、T ④
、D、T ④![]() 和
和 (核内15个中子)
(核内15个中子)
⑤CH3CH2OH和CH3OCH3 ⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com