
下列说法错误的是
A. Na2O2可用作供氧剂
B. Al2O3可用作耐火材料
C. 地沟油经处理后可用作燃料油
D. 胶体和溶液的本质区别是胶体具有丁达尔现象
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源:2017届四川省广元市高三第二次高考适应性统考理综化学试卷(解析版) 题型:选择题
25℃时,0.1molNa2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关溶液中离子浓度关系叙述正确的是
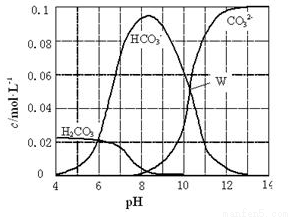
A. W点所示的溶液中:c (Na+)+c (H+)=2c(CO32- )+c (OH-)+c (Cl-)
B. pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3-)= c (OH-)+c (Cl- )
C. pH= 4的溶液中:c (H2CO3)+c (HCO3-)+c (CO32-)<0.1mol·L-1
D. pH=11的溶液中:c (Na+)>c (Cl-)>c (CO32- )>c (HCO3- )>c (H2CO3)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考化学试卷(解析版) 题型:简答题
下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:
A | |||||||||||||
B | C | D | |||||||||||
E | F | G |
(1)画出C的原子结构示意图:_________________。
(2)E在元素周期表中的位置是_________________。
(3)B、C、D、F四种元素所形成的气态氢化物最稳定的是_____________(填化学式)。
(4)E、F、G元素的最高价氧化物对应水化物的酸性最强的是_____________(填化学式)。
(5)A、B、G三元素形成的化合物的电子式是________________,其中所含的化学键有哪些类型________________。
(6)B的最高价氧化物的水化物的稀溶液与金属铜反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考化学试卷(解析版) 题型:选择题
已知某粒子AzRn+,则元素R原子的电子数为( )
A. Z B. A-Z C. A-Z+n D. A-Z-n
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三下学期第一次统测理综化学试卷(解析版) 题型:选择题
常温下,某溶液X由Fe3+、SO42-、Cu2+、Na+、CO32-、Al3+中的几种离子组成。取少量待测液滴加KSCN溶液,溶液变红;另取少量待测滴加NaOH溶液至pH=4后过滤,向滤液中继续滴加NaOH溶液至过量时又得到沉淀W和溶液Y。可能用到的数据如下表所示,下列说法正确的是
沉淀物 | Fe(OH)3 | Cu(OH)2 | Al(OH)3 |
开始沉淀的pH | 1.9 | 4.7 | 3.4 |
沉淀完全的pH | 3.2 | 6.7 | 4.7 |
A. 该温度下Ksp[Fe(OH)3]=1×10-14.6
B. W主要含有 Cu(OH)2和Al(OH)3
C. 溶液X中一定含有Cu2+、Fe3+和SO42-
D. 取溶液Y进行焰色反应,可判断溶液X中是否含有Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:选择题
将ag Fe2O3和Al2O3的混合物溶解在过量的200 ml 浓度为0.1 mol/L 的盐酸溶液中,然后向其中加入NaOH溶液,使Fe3+ 、Al3+ 刚好完全沉淀,用去NaOH溶液100ml ,则NaOH溶液的浓度为 ( )
A. 0.1mol/L B. 0.2mol/L C. 0.4mol/L D. 0.8mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列实验设计可行的是( )
A. 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
B. 加盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
C. 用萃取的方法分离汽油和煤油
D. 用溶解、过滤的方法分离KNO3和NaCl固体混合物
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市、崇左市高三联合调研考试理科综合化学试卷(解析版) 题型:简答题
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物。有关反应的热化学方程式如下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)= H2O(l)△H=-44kJ/mol
I.写出CH3OH(l)不完全燃烧生成CO和H2O(l)的热化学方程式:_________________。
II. 工业上可用CO和H2制取甲醇:CO(g)+2H2(g)=CH3OH(g) △H=akJ/mol。为研究该反应平衡时CO转化率与反应物投料比(反应物投料比=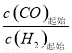 )以及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并依反应数据绘出下图:
)以及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并依反应数据绘出下图:
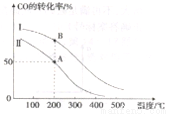
回答下列问题:
(1)反应热a____0(填“>”或“<”),判断理由是______。
(2)在其他条件相同,曲线I、II分别表示反应物投料比不同时的反应过程曲线。
①反应物投料比I_____II(填“>”或“<” 或“=”)。
②若按曲线II反应,n(CO)起始=10mol,反应物投料比=0.5,则A点的平衡常数(Ka)值为____,B点的平衡常数(Kb)值为________________。
(3)为提高CO的转化率,除了可以适当改变反应物与生成物的浓度外,还可以采取的措施有:________________、_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一3月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
A. 标准状况下,2.24 LSO3含有的分子数为0.1NA。
B. 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA。
C. 1 molFe溶于过量硝酸,电子转移数为2NA。
D. 2.0gH218O与D2O的混合物中所含中子数为NA 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com