
A、溴乙烷与6mol/L的氢氧化钠水溶液共热:C2H5Br+OH-
| |||
| B、等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:Ca2++HCO3-+OH-═CaCO3↓+H2O | |||
| C、在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1-2滴盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |||
D、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
|
| △ |
| 催化剂 |
| 500℃.30MPa |


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
| A、①②④ | B、①②③⑤ |
| C、②③ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
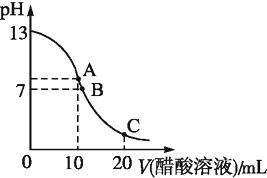 25℃时,在20mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
25℃时,在20mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )| A、在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-)) |
| C、在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D、在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
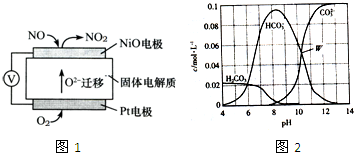 根据化学反应原理,回答下列问题:
根据化学反应原理,回答下列问题:c(HC
| ||
c(C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Na+、NO3-、Cl- |
| B、Na+、K+、Cu2+、SO42- |
| C、K+、Ca2+、HCO3-、Cl- |
| D、Mg2+、Fe3+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N4属于一种新型的化合物 |
| B、N4和N2互为同位素 |
| C、N4与N2互为同素异形体 |
| D、1molN4气体转变为N2将吸收882kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
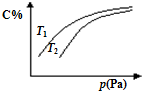 在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )| A、若正反应方向△H<0,则T1>T2 |
| B、压强增大时,混合气体的密度减小 |
| C、A一定为气体 |
| D、B一定为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
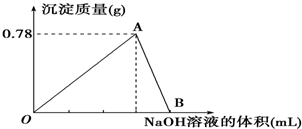 向20mL某物质的量浓度的AlCl3溶液中滴加2mol?L-1的NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向20mL某物质的量浓度的AlCl3溶液中滴加2mol?L-1的NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com