
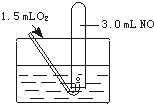
 如图所示,室温下向盛有3.0mL NO的试管中缓缓通入1.5mL O2(所有气体体积均在标准状下测定).
如图所示,室温下向盛有3.0mL NO的试管中缓缓通入1.5mL O2(所有气体体积均在标准状下测定).| 4 |
| 3 |
| 4 |
| 3 |


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
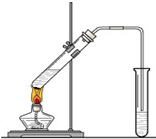 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |
| 硝酸银 |
| 氢氧化钠 |
| 稀H2SO4 |
| ||
| △ |
| ||

| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学必修一4.3 硫和氮的氧化物练习卷(解析版) 题型:计算题
如图所示,室温下向盛有3.0mLNO的试管中缓缓通入1.5mLO2(所有气体均在标准状况下测定)。
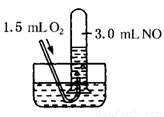
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
①___________________________________________________;
②___________________________________________________;
③___________________________________________________。
(2)最终试管中剩余的气体是________,体积为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com