
【题目】烧杯中盛有100 mL1mol/L的NaHSO4溶液,向其中逐滴滴加1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图。下列说法中正确的是( )
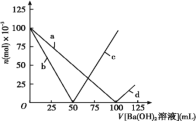
A.曲线d表示Na+的物质的量的变化
B.曲线c表示OH-的物质的量的变化
C.加入Ba(OH)2溶液50 mL反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.加入Ba(OH)2溶液大于50mL后,反应的离子方程式为:OH-+H+=H2O
【答案】B
【解析】
100mL0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,当氢氧化钡溶液体积小于50mL时,发生反应:2NaHSO4+ Ba(OH)2=BaSO4↓+2H2O+Na2SO4,当氢氧化钡溶液体积大于50mL后,硫酸氢钠中氢离子反应完全,再加入氢氧化钡溶液后发生反应:Na2SO4+ Ba(OH)2=BaSO4↓+2NaOH,直至Ba(OH)2溶液过量,硫酸根离子反应完全,据此进行解答。
A. 由图象曲线变化可知,在加入的氢氧化钡溶液体积小于100mL前,曲线a表示离子的浓度减小,此段曲线a表示的是硫酸根离子,当Ba(OH)2溶液体积大于100mL后,曲线d表示的是钡离子浓度,此反应过程中,Na+的物质的量始终未变,A项错误;
B. 由图可知c曲线表示50mLBa(OH)2溶液加入时为0,50mL以后,曲线c表示的离子浓度不断增大,则直线c表示OH的物质的量的变化,B项正确;
C. 加入Ba(OH)2溶液50mL,反应的化学方程式为:2NaHSO4+Ba(OH)2=BaSO4↓+2H2O+Na2SO4,离子方程式为:Ba2++2OH+2H++SO42=BaSO4↓+2H2O,C项错误;
D. 加入Ba(OH)2溶液大于50mL后,硫酸氢钠中氢离子已经反应完全,此时的反应为钡离子与硫酸根离子反应生成硫酸钡的反应,反应的离子方程式为:Ba2++SO42=BaSO4↓,D项错误;
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4NA个电子
B.1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C.标准状况下,22.4 L盐酸含有NA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某结晶水合物的化学式为R·nH2O,其相对分子质量为M。25℃时,ag该晶体能够溶于bg水中形成V mL饱和溶液。下列关系中不正确的是( )
A.该溶液的密度为ρ=![]() g·L-1
g·L-1
B.该溶液的物质的量浓度为c=![]() mol·L-1
mol·L-1
C.该溶液中溶质的质量分数为w=![]() %
%
D.25℃时R的溶解度S=![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空

(1)A的结构简式是____________________
(2)①的反应类型是_________________。③的反应类型是__________________。
(3)反应④的化学方程式是 ____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值,下列叙述正确的是( )
表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有![]() 个氩原子的氩气在标准状况下的体积约为22.4L
个氩原子的氩气在标准状况下的体积约为22.4L
B.标准状况下,11.2L![]() 含有的分子数为0.5
含有的分子数为0.5![]()
C.在常温常压下,11.2 L ![]() 含有的分子数为0.5
含有的分子数为0.5![]()
D.常温下,0.1mol/L NH4NO3溶液中NO3-的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
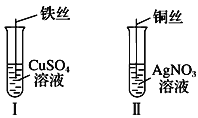
①Ⅰ中发生反应的离子方程式为______________;
②Ⅱ中铜丝上观察到的现象是_____________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为________。
(2)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是__,被氧化的元素是____,氧化剂是____,还原剂是__,氧化产物是____,还原产物是_____。
(3)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应物中氧化产物是_____;若反应中转移了0.3 mol电子,则还原产物的质量是____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定 0.1 mol/LNa2SO3溶液先升温再降温过程中的 pH ,数据如下。

实验过程中,取①、④时刻的溶液,加入盐酸酸化的 BaCl2 溶液做对比实验,④产生白色沉淀多。下列说法不正确的是( )
A. 此实验中 Na2SO3溶液的 pH 是由 pH 计测定的
B. ④与①的 PH 不同,是由于 SO32—浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的 KW值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与“物质的量”相关的计算正确的是
A.a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为![]()
B.28 g CO和22.4 L CO2中含有的碳原子数一定相等
C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D.现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com