
| A. |  制NH3 | B. | 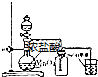 制Cl2 | C. | 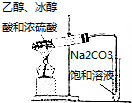 制乙酸乙酯 | D. | 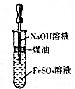 制Fe(OH)2 |
分析 A.铵盐与碱加热可制备氨气,氨气的密度比空气的密度小,利用向下排空气法收集;
B.浓盐酸与二氧化锰反应需要加热;
C.试剂应为冰醋酸,且导管在碳酸钠溶液液体下可发生倒吸;
D.煤油的密度小,在上层可隔绝氧气.
解答 解:A.铵盐与碱加热可制备氨气,氨气的密度比空气的密度小,利用向下排空气法收集,图中装置可制备氨气,故A正确;
B.浓盐酸与二氧化锰反应需要加热,图中缺少酒精灯,故B错误;
C.试剂应为冰醋酸,且导管在碳酸钠溶液液体下可发生倒吸,则不能制备乙酸乙酯,故C错误;
D.煤油的密度小,在上层可隔绝氧气,图中装置可制备Fe(OH)2,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质制备原理及装置为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
 根据如图的物理模型,回答问题:
根据如图的物理模型,回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
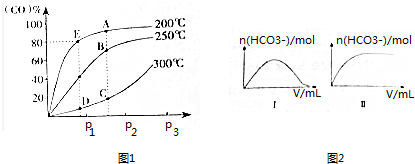
| H2CO3 | H2C2O4 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=5.4×10-2 K2=5.3×10-5 | K=7.2×10-4 | K=2.9×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
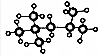 ,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;
,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
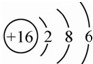 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,3.36L SO3含有的原子数目为0.6NA | |
| B. | 1 molNa2O2与足量的水反应,转移的电子数为2NA | |
| C. | 在常温常压下,13.8克NO2与足量水充分反应,剩余气体的分子数为0.1NA | |
| D. | 在1 L lmol•L-1的氨水中,含有的NH3与NH3•H2O分子的总数等于1 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com