
【题目】在10 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)该反应为____________(填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K =_________________________________。
(3)能说明该反应达到化学平衡状态的是________________(填字母)。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,
测得 c(CO) = 0.0080 mol/L ,则CO2的转化率为______________。
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ___________℃。
【答案】(1)吸热 (2)![]() (3)bc (4)80% (5)830
(3)bc (4)80% (5)830
【解析】
试题(1)影响化学平衡常数的外界因素为温度,升高温度,平衡向吸热的方向移动。由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,(2)化学平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则该反应的化学平衡常数表达式为K =![]() ;(3)a.该反应是一个反应前后体积不变的反应,容器内气体物质的量和压强不随反应的进行而变化,容器中压强不变不能说明该反应达到化学平衡状态,错误;b.化学平衡时,各组分的浓度不随时间的改变而改变,混合气体中 c(CO)不变,反应已达平衡状态,正确;c.化学平衡状态的标志是v正=v逆,所以υ正(H2)=υ逆(H2O)表明反应达到平衡状态,正确;D、化学平衡时,各组分的浓度不随时间的改变而改变,但各物质的浓度不一定相等,c(CO2)=c(CO)时,不能说明反应达到平衡状态,错误,选bc;(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO) =" 0.0080" mol﹒L-1 ,CO的物质的量为0.085mol,根据反应方程式知参加反应的CO2的物质的量为0.085mol,则CO2的转化率为85%;(5)平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),平衡常数等于1,根据表中数据判断温度是830℃。
;(3)a.该反应是一个反应前后体积不变的反应,容器内气体物质的量和压强不随反应的进行而变化,容器中压强不变不能说明该反应达到化学平衡状态,错误;b.化学平衡时,各组分的浓度不随时间的改变而改变,混合气体中 c(CO)不变,反应已达平衡状态,正确;c.化学平衡状态的标志是v正=v逆,所以υ正(H2)=υ逆(H2O)表明反应达到平衡状态,正确;D、化学平衡时,各组分的浓度不随时间的改变而改变,但各物质的浓度不一定相等,c(CO2)=c(CO)时,不能说明反应达到平衡状态,错误,选bc;(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO) =" 0.0080" mol﹒L-1 ,CO的物质的量为0.085mol,根据反应方程式知参加反应的CO2的物质的量为0.085mol,则CO2的转化率为85%;(5)平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),平衡常数等于1,根据表中数据判断温度是830℃。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 3mol H2与1 molN2混合反应生成NH3,转移电子的数目小于6×6.02×1023
B. 反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 氢氧燃料电池放电时化学能全部转化为电能
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应是为了更好的利用化学反应。回答下列问题:
(1)在①置换反应 ②化合反应 ③分解反应 ④复分解反应四种基本反应类型中,一定属于氧化还原反应的是____(填标号)。
(2)在下列反应中:K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O,___是氧化剂,___元素被氧化,___是还原产物,___是氧化产物。用双线桥标明电子转移的方向和数目:____。
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为应对全球石油资源口益紧缺。提高煤的利用效率,我国开发了煤制烃技术,并进入工业化试验阶段。
(1)煤气化制合成气(CO和H2):C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ/mol该反应在高温下能自发进行,理由是_____________。
(2)由合成气制甲醇:合成气CO和H2在一定条件下能发生如下反应:
主反应I.CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
反应II.CO(g)+H2(g)![]() C(s)+H2O(g)
C(s)+H2O(g)
①在容积均为VL的甲、乙、丙三个密闭容器中分别充入amolCO和2 amolH2,三个容器的反应温度分别为T1、T2、T3(T1<T2<T3)且恒定不变,若只发生反应I,在其他条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图所示,此时三个容器中一定处于化学平衡状态的是_____(填“T1”、“T2”或“T3”):该温度下的化学平衡常数为_____(用a、V表示)。

②为减弱副反应的发生,下列采取的措施合理的是______。
A.反应前加入少量的水蒸气 B.增压
C.降低反应温度 D.使用合适催化剂,提高甲醇的选择性
(3)由甲醇制烯烃
主反应:i.2CH3OH![]() C2H4+2H2O
C2H4+2H2O
ii.3CH3OH![]() C3H6+3H2O
C3H6+3H2O
副反应:iii.2CH3OH![]() CH3OCH3+H2O
CH3OCH3+H2O
某实验室控制反应温度为400℃,在相同的反应体系中分别填装等量的两种催化剂(Cat.1和Cat.2),以恒定的流速通入CH3OH,在相同的压强下进行两种催化剂上甲醇制烯烃的对比研究。得到如图实验数据:(选择性:转化的甲醇中生成乙烯和丙烯的百分比)
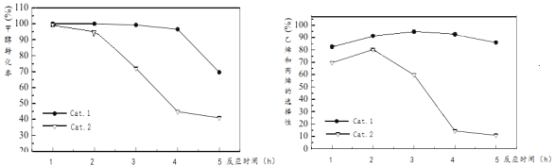

下列说法不正确的是_________。
A.反应进行一段时间后甲醇的转化率减小,可能的原因是催化剂失活,工业生产中需定期更换催化剂
B.使用Cat.2反应2h后乙烯和内烯的选择性下降,可能的原因是生成副产物二甲醚
C.使用Cat.1产生的烯烃主要为丙烯,使用Cat.2产生的烯烃主要为乙烯
D.不管使用Cat.1还是使用Cat.2都能提高活化分子的百分数
(4)已知:2CrO42-+2H+![]() Cr2O72-+H2O。以铬酸钾为原料,电化学法备重铬酸钾的实验装置示意图如下
Cr2O72-+H2O。以铬酸钾为原料,电化学法备重铬酸钾的实验装置示意图如下

①a为电源的________(填“正极”或“负极”)
②该制备过程总反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林的结构简式如右图: 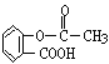
根据这一信息,回答下列问题:。
(1) 写出阿司匹林的分子式:______________________________________
(2) 根据结构,推测阿司匹林的性质,下列试剂中,不能与阿司匹林反应的是 (_______)
A、氢氧化钠溶液 B、硫酸钠溶液 C、碳酸钠溶液 D、稀硫酸
(3) 阿司匹林是一种人工合成药物,化学上用水杨酸与乙酸酐(CH3CO)2O反应来制取阿司匹林。请用化学反应方程式表示这个过程:__________________________________________________________
(4)阿司匹林与NaOH反应可以得到可溶性钠盐,有比阿司匹林更好的疗效。请写出此反应的方程式:__________________________________________________________
(5) 有四种常见药物 ①阿司匹林 ②青霉素 ③胃舒平 ④麻黄碱。请回答:
①某同学胃酸过多,应选用的药物是________(填序号)。
抗酸药是治疗胃酸过多的一类药品,请写出一种抗酸药与胃酸反应的化学方程式:_________________________________________________________
②由于具有兴奋作用,国际奥委会严禁运动员服用的药物是________(填序号)。
③从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是________(填序号)。
④滥用药物会导致不良后果,如过量服用________(填序号)会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有CO和CO2的混合气体20克,其在标准状况下的体积为11.2L。据此回答下列问题:
(1)该混合气体总的物质的量为______,其平均摩尔质量为_______。
(2)混合气体中碳原子的个数为________。(用NA表示阿伏加德罗常数的值)
(3)若将该混合气体全部通过下图装置进行实验。

则:①气球中收集的气体是______,其质量为_______ 克
②从A瓶中获得沉淀质量的操作是_____、称量。
③若要证明A瓶溶液中的阳离子是否沉淀完全,其方法为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是

A. 电池总反应为:N2H4+2O2=2NO+2H2O
B. 电池内的O2-由电极乙移向电极甲
C. 当甲电极上有lmol N2H4消耗时,乙电极上有22.4LO2参与反应
D. 电池正极方程式为:O2 + 4e-+2H2O=4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com