
【题目】下列关于铁及其化合物的说法正确的是( )
A. 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红,可以检验Fe(NO3)2晶体是否已氧化变质
B. 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C. 1 mol FeI2与足量氯气反应时转移的电子数为2NA
D. 水溶液中Fe2+、H+、SO![]() 、ClO-不能大量共存
、ClO-不能大量共存
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(含单质碳)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 .
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.
①甲同学认为X中除Fe3+外还可能含有Fe2+ . 若要确认其中的Fe2+ , 应先用(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:Br2+SO2+2H2O═H2SO4+2HBr,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g.由于此推知气体Y中SO2(标准状况下)的体积为 .
(3)[探究二]
分析上述实验中SO2体积的结果,丙同学认为气体Y中还可能含量有H2和CO2气体.为此设计了下列探究实验装置(图中夹持仪器省略).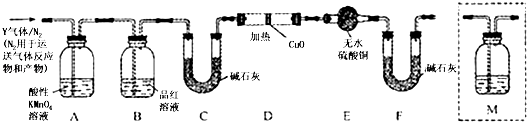
装置B中试剂的作用是 .
(4)认为气体Y中还含有CO2的理由是(用化学方程式表示).
(5)为确认CO2的存在,需将M(装有澄清石灰)添加于 (选填序号).
a.A之前 b.A~B间 c.B~C间 d.C~D间
(6)如果气体Y中含有H2 , 预计实验现象应是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
催化剂能改变化学反应的速率,原因是改变化学反应的路径.某同学在实验中发现,向2mL5%H2O2溶液中分别滴入FeCl3和FeCl2溶液,都立即产生大量气泡;向反应后的溶液中滴入几滴KSCN溶液,溶液均变为红色.查阅资料知:FeCl3在H2O2分解中发生如下反应:
①2Fe3++H2O2═2Fe2++2H++O2↑ ②2Fe2++2H++H2O2═2Fe3++2H2O
(1)在反应①中Fe3+作;在反应②中Fe3+是 . 有同学认为Fe2+也可作H2O2分解的催化剂,你认为该观点是否正确,并简述理由
.
(2)反应2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,加入少许MnSO4固体能明显观察到溶液紫色褪去时间变短.在试管中加入4mL0.01mol/LKMnO4酸性溶液和2mL0.1mol/LH2C2O4溶液,实验初始阶段时间﹣速率图象合理的是图1中的(填序号). 
(3)某反应体系中存在A、B、C、D四种物质,反应过程中各物质的物质的量变化如图2所示,请写出该反应的化学方程式 .
(4)焙烧明矾产生的SO2可用于制硫酸.已知25℃、101kPa时:
2SO2(g)+O2(g)═2SO3(g)△H1=﹣197kJmol﹣1;
H2O(g)═H2O(l)△H2=﹣44kJmol﹣1;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545kJmol﹣1 .
则SO3(g)与H2O(l)反应的热化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列有关叙述正确的是
为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,22.4LH202中含有共价键的数目为3![]()
B. 4.6g甲苯(C7H8)和丙三醇(C3H803)的混合物中含有的氢原子数为0.4![]()
C. 50mL18.4molL-1浓硫酸与足量铜微热反应,转移的电子数目为0.92![]()
D. 已知 S02(g)+l/202(g)=S03(g) △H=-98.32 KJ.mol-1,则向容器中充入![]() 个 S02分子和0.5
个 S02分子和0.5![]() 个02分子在一定条件下充分反应,最终放出的热量为98.32 kJ
个02分子在一定条件下充分反应,最终放出的热量为98.32 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g)+3Y(g)![]() 2Z(g),有关下列图像的说法不正确的是( )
2Z(g),有关下列图像的说法不正确的是( )

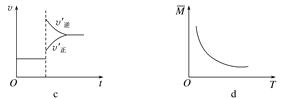
A. 依据图a可判断正反应为放热反应
B. 在图b中,虚线可表示使用了催化剂
C. 若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动
D. 由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】巴豆酸的结构简式为CH3-CH=CH-COOH。现有①氯化氢、②溴水、③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,判断在一定条件下,能与巴豆酸反应的物质是
A.全部B.只有①③④C.只有②④⑤D.只有①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com