
【题目】某同学利用下图所示装置制备乙酸乙酯。实验如下:
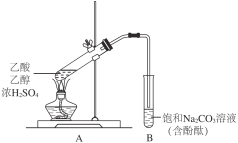
Ⅰ.向2 mL浓H2SO4和2 mL乙醇混合液中滴入2 mL乙酸后,加热试管A;
Ⅱ.一段时间后,试管B中红色溶液上方出现油状液体;
Ⅲ.停止加热,振荡试管B,油状液体层变薄,下层红色溶液褪色。
(1)为了加快酯化反应速率,该同学采取的措施有_____________。
(2)欲提高乙酸的转化率,还可采取的措施有_______________。
(3)试管B中溶液显红色的原因是___________(用离子方程式表示)。
(4)Ⅱ中油状液体的成分是__________。
(5)Ⅲ中红色褪去的原因,可能是酚酞溶于乙酸乙酯中。证明该推测的实验方案是_____________。
【答案】加热,使用催化剂 增加乙醇的用量 CO32-+H2O![]() HCO3-+OH- 乙酸乙酯、乙酸、乙醇(水) 取褪色后的下层溶液,滴加酚酞试液,溶液变红
HCO3-+OH- 乙酸乙酯、乙酸、乙醇(水) 取褪色后的下层溶液,滴加酚酞试液,溶液变红
【解析】
(1)酯化反应是可逆反应,可根据影响化学反应速率的因素分析;
(2)根据酯化反应是可逆反应,要提高乙酸转化率,可以根据该反应的正反应特点分析推理;
(3)根据盐的水解规律分析;
(4)根据乙酸、乙醇及乙酸乙酯的沸点高低分析判断;
(5)红色褪去的原因若是由于酚酞溶于乙酸乙酯中所致,则可通过向溶液中再加入酚酞,观察溶液颜色变化分析。
(1)酯化反应是可逆反应,由于升高温度,可使化学反应速率加快;使用合适的催化剂,可以加快反应速率,或适当增加乙醇的用量,提高其浓度,使反应速率加快等;
(2)乙酸与乙醇在浓硫酸催化作用下加热,发生酯化反应产生乙酸乙酯和水,反应产生的乙酸乙酯和水在相同条件下又可以转化为乙酸与乙醇,该反应是可逆反应,要提高乙酸的转化率,可以通过增加乙醇(更便宜)的用量的方法达到;
(3)碳酸钠是强碱弱酸盐,在溶液中,CO32-发生水解反应,消耗水电离产生的H+转化为HCO3-,当最终达到平衡时,溶液中c(OH-)>c(H+)所以溶液显碱性,可以使酚酞试液变为红色,水解的离子方程式为:CO32-+H2O![]() HCO3-+OH-;
HCO3-+OH-;
(4)乙酸与乙醇在浓硫酸催化作用下加热,发生酯化反应产生乙酸乙酯和水,由于反应产生乙酸乙酯的沸点比较低,且反应物乙酸、乙醇的沸点也都不高,因此反应生成的乙酸乙酯会沿导气管进入到试管B中,未反应的乙酸和乙醇也会有部分随乙酸乙酯进入到B试管中,因此Ⅱ中油状液体的成分是乙酸乙酯、乙酸、乙醇(水);
(5)红色褪去的原因若是由于酚酞溶于乙酸乙酯中所致,则可通过取褪色后的下层溶液,滴加酚酞试液,若溶液变红证明是酚酞溶于乙酸乙酯所致。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】关于化合物2苯基丙烯(![]() ),下列说法正确的是
),下列说法正确的是
A. 不能使稀高锰酸钾溶液褪色
B. 可以发生加成聚合反应
C. 分子中所有原子共平面
D. 易溶于水及甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.破坏乙烯分子里![]() 所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
B.乙烯分子和苯分子都能使溴水褪色,两者褪色原理相同
C.因为甲烷和苯都不能被酸性 KMnO4 溶液氧化,所以两者都不能发生氧化反应
D.甲烷和苯都能和氯气发生取代反应,但是两者发生反应时需要的条件不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 A、B 置于固定容积为 1L 的密闭容器中,发生反应:3A(g)+B(g)2C(g)+2D(g),反应进行到 10 s 末,测得 A 的物质的量为 1.8 mol,B 的物质的量为 0.6 mol,C 的物质的量为 0.8 mol,下列说法错误的是( )
A.用 C 表示 10 s 内反应的平均反应速率为 0.8 molL-1s-1
B.反应前 A 的物质的量浓度是 3 molL-1
C.10 s 末,生成物 D 的物质的量为 0.8 mol
D.保持其他条件不变,适当升高温度,正逆反应速率都加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧法是测定有机物分子式的一种重要方法。完全燃烧 0.1mol 某烃后,测得生成的二氧化碳为 11.2 L(标准状况),生成的水为 10.8g。请完成下面的填空:
(1)该烃的分子式为_________。
(2)写出它可能存在的全部物质的的结构简式 :_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1molCl2发生反应时,转移的电子数一定为2NA
B.1.7g H2O2中含有的电子数为0.9 NA
C.1mol Na2O2 固体中含离子总数为4 NA
D.标准状况下,2.24L苯所含分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
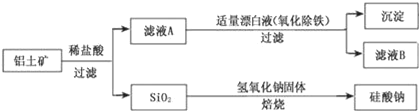
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:__Fe2+___ClO-+( )___=____Fe(OH)3↓+__C1﹣+( )。
②检验滤液B中是否还含有铁元素的方法为:________(注明试剂、现象)。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、____(填操作名称)、洗涤。
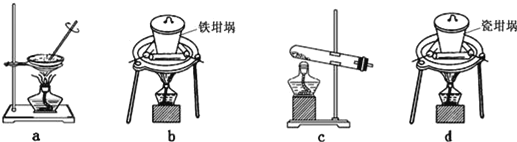
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlH3是一种储氢材料,可作为固体火箭推进剂。通过激光加热引发AlH3的燃烧反应,燃烧时温度随时间变化关系如下图所示。燃烧不同阶段发生的主要变化如下:
2AlH3(g)=2Al(s)+3H2(g) △H1 H2(g)+![]() O2(g)=H2O(g) △H2 Al(s)= Al(g) △H3 Al(g) +
O2(g)=H2O(g) △H2 Al(s)= Al(g) △H3 Al(g) +![]() O2(g)=
O2(g)=![]() Al2O3(s) △H4
Al2O3(s) △H4
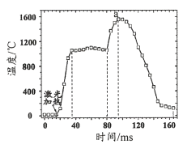
下列分析正确的是
A.AlH3燃烧需要激光加热引发,所以AlH3燃烧是吸热反应
B.其他条件相同时,等物质的量的Al(s)燃烧放热大于Al(g)燃烧放热
C.在反应过程中,a点时物质所具有的总能量最大
D.2AlH3(s)+3O2(g)=Al2O3(s)+3H2O(g) △H=△H1+3△H2+2△H3+2△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )

A. A、B、D可能是钠及其化合物 B. A、B、D可能是镁及其化合物
C. A、B、D可能是铝及其化合物 D. A、B、D可能是非金属及其化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com