
I��ijѧ����0.2000 mol��L��1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
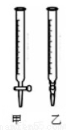
��������ˮϴ�Ӽ�ʽ�ζ��ܣ���ע��NaOH��Һ����0���̶�������
�ڹ̶��õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0����0���̶������£������¶���
����ȡ20.00mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�����
��ش�
��1�����ϲ����д�����ǣ����ţ� ��
��2���ñ�NaOH��Һ�ζ�ʱ��Ӧ����NaOH��Һע��______�С�����ͼ��ѡ��ס����ҡ���
��3�����в���������ʵ����ƫ����ǣ�______�����ţ�
A������ƿװҺǰ��������������ˮ
B���ζ�ǰ���ζ��ܼ��������ݣ��ζ���������
C����ƿ��������ˮϴ�Ӻ�δ�ô���Һ��ϴ
D������ʽ�ζ�����ȡҺ��ʱ���ͷ�Һ��ǰ�ζ���ǰ�������ݣ�֮����ʧ
��4���ζ�ʱ�����ֿ��Ƶζ��ܣ�����ҡ����ƿ���۾�ע�� ���жϵ���ζ��յ�������ǣ���ƿ����Һ ��
��5��������ʵ�����ݼ�¼��
�ζ����� | �������mL | NaOH��Һ���������mL�� | |
�ζ�ǰ | �ζ��� | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
ͨ������ɵã�������Ũ��Ϊ��______ mol•L-1������������4λС����
II�����ü�����ζ����ɲⶨBa2���ĺ�����ʵ����������С�
��֪��2CrO42����2H����Cr2O72����H2O Ba2����CrO42����BaCrO4��
����1����ȡx mLһ��Ũ�ȵ�Na2CrO4��Һ����ƿ�У��������ָʾ������b mol��L��1�����Һ�ζ����յ㣬��õμ��������ΪV0 mL��
����2����ȡy mL BaCl2��Һ����ƿ�У�����x mL�벽��:1��ͬŨ�ȵ�Na2CrO4��Һ����Ba2����ȫ�������ټ������ָʾ������b mol��L��1�����Һ�ζ����յ㣬��õμ���������ΪV1 mL��
��BaCl2��ҺŨ��Ϊ______________________ mol��L��1��������2�еμ�����ʱ����������Һ��������Ba2��Ũ�ȵIJ���ֵ��___________���ƫ��ƫС������
���𰸡�I����1���٢ܣ���2���ң���3��B��
��4����ƿ����ɫ������ɫ���dz��ɫ���Ұ�����ڲ���ɫ����5��0.1631��
II����V0b��V1b��/y ��ƫ��
��������
�����������1���ٸ��ݼ�ʽ�ζ�����װҺǰӦ����װҺ�������ϴ��������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶������ϣ���ʽ�ζ���δ�ñ�����������Һ��ϴ��ֱ��ע���NaOH��Һ����Һ��Ũ��ƫС�����V������ƫ����c�����⣩=V(��)��c(��) ��V(����)����֪c������ƫ�����ָʾ����̪��������ʣ�Ҳ�ᷴӦ�������Ϊ�˼���ʵ������̪һ��μ�1�λ�2�Σ��������������ȷ����2��NaOH�Ǽ�����벣���е�SiO2������Ӧ������Ӧ��װ�ڼ�ʽ�ζ������У���3��A������ƿװҺǰ��������������ˮ�����ڲ�Ӱ���ᡢ������ʵ��������ԶԵζ�������Ӱ�죬����B���ζ�ǰ���ζ��ܼ��������ݣ��ζ��������ݣ�ʹ����Һ���ƫ���´�����Һ��Ũ��ƫ�ߣ���ȷ��C����ƿ��������ˮϴ�Ӻ�δ�ô���Һ��ϴ��������ȷ���������������D������ʽ�ζ�����ȡҺ��ʱ���ͷ�Һ��ǰ�ζ���ǰ�������ݣ�֮����ʧ���������Һ���ƫ�٣���Ӧ���ı�����Һ�����ƫС��ʹ���Ũ��ƫ�ͣ�����4���ζ�ʱ�����ֿ��Ƶζ��ܣ�����ҡ����ƿ���۾�ע����ƿ����ɫ���жϵ���ζ��յ�������ǣ���ƿ����Һ����ɫ���dz��ɫ���Ұ�����ڲ���ɫ����5�������кͷ�Ӧʱ���ߵ����ʵ�����ȡ�����ʵ�����ݿ�֪����һ��ʵ���������̫��������V(NaOH)= (16.30+16.32)��2=16.31mL��c(NaOH)��V(NaOH)=c(HCl)��V(HCl),����c(HCl)=[ c(NaOH)��V(NaOH)]��V(HCl)= [0.2000 mol��L��1��16.31mL]��20.00mL=0.1631mol/L��II�����ݷ���ʽ��֪�����ӵ����ʵ�������Һ��Ba2+�����ʵ�����ȡ������Ba2+��ȫ�������ټ������ָʾ������b mol•L-1�����Һ�ζ����յ㣬��õμ���������ΪV1 mL������2CrO42����2H����Cr2O72����H2O����������ʵ���Ϊ��V1��10-3��bmol���������b mol•L-1�����Һ�ζ����յ㣬��õμ��������ΪV0 mL�����������������ʵ�����V0��10-3��bmol��Ba2����CrO42����BaCrO4������Ba2+��Ӧ��CrO42�������ʵ���ΪV0��10-3��bmol-V1��10-3��bmol=��V0 -V1��b��10-3mol���������ȡy mLBaCl2��Һ����ƿ�У�����BaCl2��Һ��Ũ��Ϊ����V0 -V1��b��10-3mol ��y��10?3mol/L=��V0b��V1b��/ymol/L����������еμ�����ʱ����������Һ������V1��С����Ba2+Ũ�Ȳ���ֵ��ƫ��
���㣺��������к͵ζ����й�֪ʶ��
�����͡�ʵ����
���������
�����⡿����ǿУ��2015-2016ѧ��������������һ�и�һ����ĩ��ѧ�Ծ�����������
���ؼ��ֱ�ǩ��
��������
��Ԫ�ص��⻯����������ڹ�ҵ�������������ж��й㷺Ӧ�ã��ش��������⣺
��1����֪��2NO2(g)  N2O(g) ��H1 2NO2(g)
N2O(g) ��H1 2NO2(g)  N2O(l) ��H2
N2O(l) ��H2
���������仯ʾ��ͼ�У���ȷ���ǣ�ѡ����ĸ�� ��

��2��������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�������ͼ��
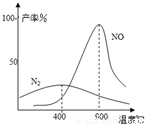
�¶Ƚϵ�ʱ������ Ϊ�����¶ȸ���900��ʱ��NO�����½���ԭ���� ��
��3�����������Ҫ���ܵ�ȼ�ϣ���������������������������N2H4����Ϊȼ�ϣ���ҵ�����ð������������Ժϳɰ��������ֿ��Խ�һ���Ʊ������ȡ�
��֪��N2(g)+2O2(g)=2NO2(g) ��H����67.7kJ•mol��1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ��H����534.0kJ•mol��1
NO2(g)  1/2 N2O4(g) ��H����26.35kJ•mol-1
1/2 N2O4(g) ��H����26.35kJ•mol-1
��д����̬��������̬������������ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ�� ��
���ð��ʹ������ư�һ�����ʵ���֮�Ȼ�Ϸ�Ӧ�������������÷�Ӧ�Ļ�ѧ����ʽΪ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
A��B���Ƿ����廯���1molAˮ��õ�1molB��1mol���ᡣA��B����Է���������������200����ȫȼ�ն�ֻ����CO2��H2O����B������̼����Ԫ���ܵ���������Ϊ65.2%��A��Һ�������ԣ�����ʹFeCl3��Һ��ɫ��
��1��A��B����Է�������֮��Ϊ ��
��2��1��B������Ӧ���� ����ԭ�ӡ�
��3��A�������Ĺ��������ƣ� ��
��4��1molB���ʷֱ���������̼��������Һ������������Һ��Ӧ���������Ķ��ߵ����ʵ���֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ӦA+B=C+D�������仯��ͼ��ʾ������˵����ȷ����
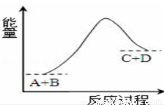
A���÷�Ӧֻ���ڼ��������²��ܽ���
B���÷�ӦΪ���ȷ�Ӧ
C���÷�ӦΪ���ȷ�Ӧ
D����Ӧ��������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ݵ���������Ӧ���Ȼ�ѧ����ʽ�������ж���ȷ����
��i��H2��g��+I2��g��==2HI��g��;��H=-9.48kJ/mol
��ii��H2��g��+I2��s��==2HI��g������H=+26.48kJ
A��1mol I2��g����ͨ��2��g��H2��g������Ӧ����9.48kJ
B��1mol I2��s������������17.00kJ
C����Ӧ��i���IJ���ȷ�Ӧ��ii���IJ����ȶ�
D����Ӧ��ii���ķ�Ӧ���������ȷ�Ӧ��i���ķ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ɫ��Һ�к��д�����H+��SO42-�������Һ���ܴ������ڵ���������
A��Na+��Fe2+��NO3- B��Na+��Mg2+��NO3-
C��Cr2O72-��Ba2+��Cl- D��K+��Na+��S2O32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ��ƶ���
����ֱ��ˮ�Ϸ����Ҵ��ķ���ʽΪ��C2H4 (g)��H2O(g)��C2H5OH(g)��������ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ[��ʼn(H2O)�Un(C2H4)=1�U1]��
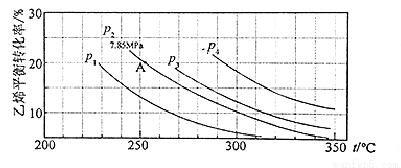
������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��KPΪ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ���������
A��0.068 MPa��1 B��0.082 C��0.072 MPa��1 D��0.082 MPa��1
���𰸡�C
��������
�����������ͼ��֪��A����ϩ��ƽ��ת����Ϊ20%������ʼ��n(H2O)=n(C2H4)=1mol��ת������ϩΪ0.2mol���� C2H4 (g)��H2O(g)��C2H5OH(g)
��ʼ����mol����1 1 0
ת������mol����0.2 0.2 0.2
ƽ������mol����0.8 0.8 0.2
ѹǿ֮�ȵ������ʵ���֮�ȣ���p(C2H4)=p(H2O)=7.8MPa��(0.8mol��1.8mol)=7.8MPa��4/9��p(C2H5OH)=7.8MPa��1/9����Kp=p(C2H5OH)/[p(C2H4)��p(H2O)]=(7.8MPa��1/9)7.8MPa��4/9��7.8MPa��4/9 =0.072MPa-1��ѡ��C��ȷ��
���㣺����ͼ���ڻ�ѧƽ������Ӧ�õ�֪ʶ��
�����͡�ѡ����
���������
�����⡿����ǿУ��2015-2016ѧ��������������һ�и�һ����ĩ��ѧ�Ծ�����������
���ؼ��ֱ�ǩ��
��������
X��Y��Z��J��Q���ֶ���������Ԫ�أ�ԭ��������������Ԫ��Z�ڵؿ��к�����ߣ�JԪ�ص���ɫ��Ӧ�ʻ�ɫ��Q�������������������������Ϊ3:8��X����J�γ����ӻ������J���İ뾶����X���İ뾶��Y2�ǿ�������Ҫ�ɷ�֮һ����ش�
��1��QԪ�������ڱ��е�λ��_______________________��
��2��������Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳��Ϊ_____________________________����Ԫ�ط��ţ���
��3��Ԫ�صķǽ�����Z____Q������������������и����У�����˵����һ���۵���ʵ�� ������ţ�
A��Q���⻯���ˮ��Һ�����ڿ����л����� |
B��Z��Q֮���γɵĻ�������Ԫ�صĻ��ϼ� |
C��Z��Q�ĵ��ʵ�״̬ |
D��Z��Q�����ڱ��е�λ�� |
��4��X��Y���γɼ���A��д��A�ĵ���ʽ_______________��ʵ�����Ʊ�����A�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ȷ����
�����Ӱ뾶��K����Al3����S2����Cl��
���⻯����ȶ��ԣ�HF��HCl��H2S��PH3��SiH4
�����ӵĻ�ԭ�ԣ�S2����Cl����Br����I��
�������ԣ�Cl2��S��Se��Te
�����ԣ�H2SO4��H3PO4��H2CO3��HClO
�ǽ����ԣ�O��N��P��Si
�߽����ԣ�Be��Mg��Ca��K
A. �ڢݢ� B. �ڢޢ� C. �ڢܢݢޢ� D. �ڢܢ�
���𰸡�C
������������������ٵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶S2����Cl����K����Al3�������ڷǽ�����F��Cl��S��P��Si���⻯���ȶ��ԣ�HF��HCl��H2S��PH3��SiH4����ȷ���۷ǽ�����Cl��Br��I��S�������ӻ�ԭ��S2����I����Br����Cl�������ܷǽ�����Cl��S��Se��Te������������Cl2��S��Se��Te����ȷ���ݷǽ�����S��P��C����ۺ����������H2SO4��H3PO4��H2CO3��̼������Ա�HClOǿ��������H2SO4��H3PO4��H2CO3��HClO����ȷ����ͬ������ԭ����������Ԫ�طǽ�������ǿ��ͬ�������϶���Ԫ�طǽ����Լ������ʷǽ�����O��N��P��Si����ȷ����ͬ�������϶��½�������ǿ��ͬ����������ҽ����Լ������ʽ����ԣ�Be��Mg��Ca��K����ȷ����ȷ���ж��Ǣڢܢݢޢ� ��ѡ��C�������⡣
���㣺�������뾶�Ƚϡ������Լ���ԭ��ǿ���Ƚϼ�ͬ���ڡ�ͬ����Ԫ�ؽ����Էǽ�����ǿ���Ƚϵ�֪ʶ��
�����͡�ѡ����
�����á�һ��
�����⡿����ǿУ��2015-2016ѧ��������������һ�и�һ����ĩ��ѧ�Ծ�����������
���ؼ��ֱ�ǩ��
��������
����ͼʾ���Ӧ�������������
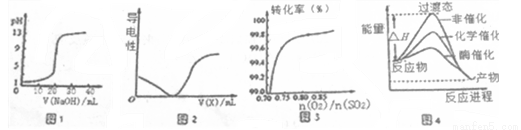
A��ͼһ��ʾ0.1000mol��L��1NaOH��Һ�ζ�20.00ml 0.1000 mol��L��1������Һ�õ��ζ�����
B��ͼ2��ʾ��H2S��Һ������ʵ���У����߿�ȷ��ͨ�������XΪCl2
C��ͼ3��������������ʱ��2SO2(g)��O2(g)  2SO3(g)ת����ϵ�У��������ʾO2��ת����
2SO3(g)ת����ϵ�У��������ʾO2��ת����
D����ͼ4��ʾ���߿�֪��ø���Ȼ�ѧ����Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
�±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺

��1�����ԭ�ӽṹʾ��ͼΪ ��
��2���ڵ���̬�⻯����ӵĽṹʽΪ �������������ˮ����ķ���ʽ ��
��3���ڡ��۵���ۺ������������ǿ������˳���� �����ѧʽ��
��4���ݡ���Ԫ�صĽ�����ǿ������ �������������С�����䡱��
��5���ܡ��ݡ����γɵļ����Ӱ뾶���� �������������С�����䡱��
��6���١��ܡ���Ԫ�ؿ��γɼȺ����Ӽ��ֺ����ۼ��Ļ����д�����ĵ���ʽ ��
��7���ݡ��ޡ��������������Ӧˮ�����������ܷ�Ӧ��д���䷴Ӧ�����ӷ���ʽ�� �� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣�������λ���ѧ��һ����ĩ�Ŀƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��������������̵��ǣ� ��
A��ú�ĸ��� B��ú������ C��ʯ�ͷ��� D��ʯ���ѻ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com