
”¾ĢāÄæ”æŌŖĖŲÖÜĘŚ±ķÖŠĒ°ČżÖÜĘŚ²æ·ÖŌŖĖŲµÄŌ×ÓŠņŹżÓė³£¼ū¼ŪĢ¬µÄ¹ŲĻµĶ¼ČēĻĀ”£ČōÓĆŌ×ÓŠņŹż±ķŹ¾¶ŌÓ¦ŌŖĖŲ£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ

A.aÓėdµÄ·Ē½šŹōŠŌ±Č½Ļ£ŗa> d
B.Ō×Ó°ė¾¶“󊔣ŗb>c>a>d>e
C.aæÉŅŌŠĪ³ÉĮ½ÖÖĒā»ÆĪļ
D.b”¢c”¢eµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÖ®¼ä¾łæÉ·“Ó¦
”¾“š°ø”æB
”¾½āĪö”æ
øł¾ŻĶ¼Ź¾æÉÖŖ£¬aĪŖO£¬bĪŖNa£¬cĪŖAl£¬dĪŖP£¬eĪŖCl”£
A”¢øł¾ŻĶ¬ÖÜĘŚ£¬“Ó×óµ½ÓŅ·Ē½šŹōŠŌŌö¼Ó£¬µĆµ½S>P£¬øł¾ŻĶ¬Ö÷×壬“ÓÉĻµ½ĻĀ·Ē½šŹōŠŌ¼õČõ£¬µĆµ½O>S£¬ĖłŅŌ·Ē½šŹōŠŌ±Č½Ļ£ŗO > P£¬¹ŹAÕżČ·£»
B”¢øł¾Ż²ć¶ą¾¶“ó£¬ŗĖ¶ą¾¶Š”(Ķ¬µē×Ó²ć½į¹¹)£¬Ō×Ó°ė¾¶“󊔣ŗNa > Al > P >Cl > O£¬¹ŹB“ķĪó£»
C”¢OæÉŅŌŠĪ³ÉĮ½ÖÖĒā»ÆĪļ£¬Ė®ŗĶ¹żŃõ»ÆĒā£¬¹ŹCÕżČ·£»
D”¢Na”¢Al”¢ClµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·Ö±šĪŖĒāŃõ»ÆÄĘ”¢ĒāŃõ»ÆĀĮ”¢øßĀČĖį£¬ĒāŃõ»ÆÄĘÓėĒāŃõ»ÆĀĮ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬ĒāŃõ»ÆÄĘŗĶøßĀČĖį·“Ӧɜ³ÉøßĀČĖįÄĘŗĶĖ®£¬ĒāŃõ»ÆĀĮŗĶøßĀČĖį·“Ӧɜ³ÉøßĀČĖįĀĮŗĶĖ®£¬¹ŹDÕżČ·£»
“š°øĪŖB”£


 æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČČ¼¤»īµē³ŲæÉÓĆ×÷»š¼ż.µ¼µÆµÄ¹¤×÷µēŌ“”£Ņ»ÖÖČČ¼¤»īµē³ŲµÄ»ł±¾½į¹¹ČēĶ¼ĖłŹ¾£¬ĘäÖŠ×÷ĪŖµē½āÖŹµÄĪŽĖ®LiCl-KCl»ģŗĻĪļŹÜČČČŪČŚŗ󣬵ē³Ų¼“æÉĖ²¼äŹä³öµēÄÜ”£øƵē³Ų×Ü·“Ó¦ĪŖ£ŗPbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb”£

ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A £®Õż¼«·“Ó¦Ź½£ŗCa+2Cl- - 2e- =CaCl2
B£®·Åµē¹ż³ĢÖŠ£¬Li+Ļņøŗ¼«ŅʶÆ
C£®³£ĪĀŹ±£¬ŌŚÕżøŗ¼«¼ä½ÓÉĻµēĮ÷±ķ»ņ¼ģĮ÷¼Ę£¬ÖøÕė²»Ę«×Ŗ
D£®Ćæ×ŖŅĘ0.1molµē×Ó£¬ĄķĀŪÉĻÉś³É20.7g Pb
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)³ąĖ®É¹“׏ĒĪŅĆĒ×ńŅåĢŲ²śÖ®Ņ»£¬ĘäÖŠŗ¬ÓŠŅ»¶ØĮæµÄCH3COOH”£Š“³öCH3COOHµÄµēĄė·½³ĢŹ½ ______£»ŌŚŅŃ“ļĘ½ŗāµÄŅŅĖįČÜŅŗÖŠ¼ÓČėŅ»¶ØµÄCH3COONa £¬øĆČÜŅŗpH_______£ØĢī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£©”£
(2)Č¼ĮĻµē³ŲĘū³µ£¬ÓČĘäŹĒĒāČ¼ĮĻµē³ŲĘū³µæÉŅŌŹµĻÖĮćĪŪČ¾”¢ĮćÅÅ·Å£¬Ēż¶ÆĻµĶ³¼øŗõĪŽŌėŅō£¬ĒŅĒāÄÜȔ֮²»¾””¢ÓĆÖ®²»½ß,Ņņ“ĖČ¼ĮĻµē³ŲĘū³µ³ÉĪŖĘū³µĘóŅµ¹Ų×¢µÄ½¹µć”£Č¼ĮĻµē³ŲµÄČ¼ĮĻæÉŅŌŹĒĒāĘų”¢¼×“¼µČ”£ÓŠæĘ¼¼¹¤×÷ÕߥūÓĆĻ”ĶĮ½šŹōŃõ»ÆĪļ×÷ĪŖ¹ĢĢåµē½āÖŹÖĘŌģ³öĮĖ¼×“¼”ŖæÕĘųČ¼ĮĻµē³Ų”£ÕāÖÖĻ”ĶĮ½šŹōŃõ»ÆĪļŌŚøßĪĀĻĀÄÜ“«µ¼O2-”£
¢ŁøƵē³ŲµÄÕż¼«·“Ó¦ŹĒ___________£»øŗ¼«·“Ó¦ŹĒ____________”£
¢ŚŌŚĻ”ĶĮŃõ»ÆĪļµÄ¹ĢĢåµē½āÖŹÖŠ£¬O2-µÄŅĘ¶Æ·½ĻņŹĒ__________”£
¢Ū¼×“¼æÉŅŌŌŚÄŚČ¼»śÖŠČ¼ÉÕÖ±½Ó²śÉś¶ÆĮ¦ĶĘ¶Æ»ś¶Æ³µŌĖŠŠ£¬¶ųæĘ¼¼¹¤×÷ÕßŅŖ»Ø·Ń“óĮæµÄ¾«Į¦ŃŠ¾æ¼×“¼Č¼ĮĻĘū³µ,Ö÷ŅŖŌŅņŹĒ___________”£
(3)ŌŚAgClµÄ±„ŗĶČÜŅŗÖŠ“ęŌŚ³ĮµķČܽāĘ½ŗā£ŗAgCl(s) ![]() Ag+(aq)+Cl-(aq)£¬ŌŚ25”ꏱ,Ksp(AgCl)£½1.8”Į10-10”£ĻÖ½«×ćĮæĀČ»ÆŅų·Ö±š·ÅČė£ŗ
Ag+(aq)+Cl-(aq)£¬ŌŚ25”ꏱ,Ksp(AgCl)£½1.8”Į10-10”£ĻÖ½«×ćĮæĀČ»ÆŅų·Ö±š·ÅČė£ŗ
¢Ł100 mLÕōĮóĖ®ÖŠ£»¢Ś100 mL 0.2 mol/L AgNO3ČÜŅŗÖŠ£»¢Ū100 mL 0.1 mol/LĀČ»ÆĀĮČÜŅŗÖŠ£»¢Ü100 mL 0.1 mol/LŃĪĖįÖŠ£¬³ä·Ö½Į°čŗó£¬ĻąĶ¬ĪĀ¶ČĻĀc(Ag£«)Óɓ󵽊”µÄĖ³ŠņŹĒ_____(ĢīŠ“ŠņŗÅ)£»ĘäÖŠ¢ŚÖŠĀČĄė×ÓµÄÅضČĪŖ______mol/L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ( )
A. ŅŅĖįÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£ŗ2H+£«CO32”Ŗ== CO2”ü£«H2O
B. “×ĖįČÜŅŗÓėŠĀÖĘĒāŃõ»ÆĶ·“Ó¦£ŗCH3COOH£«OH£”śCH3COO££«H2O
C. ±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĢ¼£ŗ2C6H5O££«CO2£«H2O ”ś2C6H5OH£«CO32”Ŗ
D. ¼×Č©ČÜŅŗÓė×ćĮæµÄŅų°±ČÜŅŗ¹²ČČ£ŗHCHO+4[Ag(NH3)2]++4OH-![]() CO32”Ŗ+2NH4++4Ag”ż+6NH3+2H2O
CO32”Ŗ+2NH4++4Ag”ż+6NH3+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ»śĪļĻą¹ŲĆčŹö²»ÕżČ·µÄ
A£®ÓĆäåĖ®ÄÜĒų·ÖŅŅĖį”¢¼ŗĻ©”¢±½”¢ĖÄĀČ»ÆĢ¼
B£®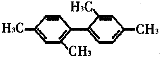 ·Ö×ÓÖŠÖĮÉŁÓŠ11øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
·Ö×ÓÖŠÖĮÉŁÓŠ11øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
C£®øŹ°±Ėį£ØH2N”ŖCH2COOH£©”¢±ū°±Ėį[CH3CH£ØNH2£©COOH]”¢¹Č°±Ėį[HOOC”ŖCH2CH2CH£ØNH2£©COOH]Ņ»¶ØĢõ¼žĻĀŠĪ³ÉĮ“דȿėĵĽį¹¹×ī¶ąÓŠ3ÖÖ
D£®1molÓŠ»śĪļ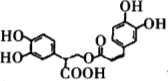 Ņ»¶ØĢõ¼žĻĀÄÜŗĶ6molNaOH·“Ó¦”£
Ņ»¶ØĢõ¼žĻĀÄÜŗĶ6molNaOH·“Ó¦”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
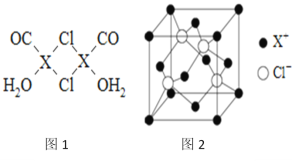
”¾ĢāÄæ”æŌŖĖŲXµÄ»łĢ¬Ō×ÓÖŠµÄµē×Ó¹²ÓŠ7øöÄܼ¶£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖ1£¬XŌ×ÓµÄÄŚ²ć¹ģµĄČ«²æÅÅĀśµē×Ó£®ŌŚĘųĢå·ÖĪöÖŠ£¬³£ÓĆXClµÄŃĪĖįČÜŅŗĪüŹÕ²¢¶ØĮæ²ā¶ØCOµÄŗ¬Į棬Ęä»Æѧ·“Ó¦ČēĻĀ£ŗ2XCl+2CO+2H2OØTX2Cl2”¤2CO”¤2H2O
£Ø1£©X»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½ĪŖ__________________£®
£Ø2£©C”¢H”¢OČżÖÖŌ×ӵĵēøŗŠŌÓɓ󵽊”µÄĖ³ŠņĪŖ__________£®
£Ø3£©X2Cl2”¤2CO”¤2H2OŹĒŅ»ÖÖÅäŗĻĪļ£¬Ęä½į¹¹ČēĶ¼1ĖłŹ¾£ŗ
¢ŁÓėCOĪŖ»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓŹĒ_________£®
¢ŚøĆÅäŗĻĪļÖŠĀČŌ×ÓµÄŌӻƷ½Ź½ĪŖ__________£®
¢ŪŌŚX2Cl22CO2H2OÖŠ£¬ĆæøöXŌ×ÓÄÜÓėĘäĖūŌ×ÓŠĪ³É3øöÅäĪ»¼ü£¬ŌŚĶ¼ÖŠÓĆ”°”ś”±±ź³öĻąÓ¦µÄÅäĪ»¼ü_____________£®
£Ø4£©°¢·ü¼ÓµĀĀŽ³£ŹżµÄ²ā¶ØÓŠ¶ąÖÖ·½·Ø£¬XÉäĻßŃÜÉä·Ø¾ĶŹĒĘäÖŠµÄŅ»ÖÖ”£Ķعż¶ŌXCl¾§ĢåµÄXÉäĻßŃÜÉäĶ¼ĻóµÄ·ÖĪö£¬æÉŅŌµĆ³öXClµÄ¾§°ūČēĶ¼2ĖłŹ¾£¬Ōņ¾ąĄėĆæøöX+×ī½üµÄCl©µÄøöŹżĪŖ____________,ČōXŌ×ӵİė¾¶ĪŖa pm£¬¾§ĢåµÄĆܶČĪŖ¦Ńg/cm3£¬ŹŌĶعż¼ĘĖć°¢·ü¼ÓµĀĀŽ³£ŹżNA=___________________(ĮŠ¼ĘĖćŹ½±ķ“ļ)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚŗćČŻČŻĘ÷ÖŠĶ¶ČėŅ»¶ØĮæ“æ¾»µÄ°±»ł¼×Ėįļ§£¬·¢ÉśĻĀĮŠ·“Ó¦NH2COONH4(s) ![]() 2NH3(g)£«CO2(g)”£ÄÜÅŠ¶ĻøĆ·Ö½ā·“Ó¦ŅŃ¾“ļµ½»ÆŃ§Ę½ŗāµÄŹĒ
2NH3(g)£«CO2(g)”£ÄÜÅŠ¶ĻøĆ·Ö½ā·“Ó¦ŅŃ¾“ļµ½»ÆŃ§Ę½ŗāµÄŹĒ
A.2v(NH3)=v(CO2)
B.ĆܱÕČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä
C.ĆܱÕČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»±ä
D.ĆܱÕČŻĘ÷ÖŠ°±ĘųµÄĢå»ż·ÖŹż²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśĻĀĮŠ·“Ó¦£ŗ![]() ·“Ó¦¹ż³ĢÖŠ£¬ø÷ĪļÖŹÅضČÓėŹ±¼äµÄ¹ŲĻµČēĶ¼£ŗ
·“Ó¦¹ż³ĢÖŠ£¬ø÷ĪļÖŹÅضČÓėŹ±¼äµÄ¹ŲĻµČēĶ¼£ŗ
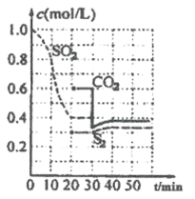
(1)øĆ·“Ó¦Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ![]() ____________”£
____________ӣ
(2)![]() »Æѧ·“Ó¦ĖŁĀŹ±ķŹ¾
»Æѧ·“Ó¦ĖŁĀŹ±ķŹ¾![]() ______£»½ØĮ¢Ę½ŗā¹ż³ĢÖŠ£¬»ģŗĻĘųĢåµÄĆܶČ______£ØŃ”Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
______£»½ØĮ¢Ę½ŗā¹ż³ĢÖŠ£¬»ģŗĻĘųĢåµÄĆܶČ______£ØŃ”Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
(3)![]() Ź±øıäĶā½ēĢõ¼ž£¬Ź¹
Ź±øıäĶā½ēĢõ¼ž£¬Ź¹![]() ______
______![]() £ØŃ”Ģī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
£ØŃ”Ģī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠNaCl”¢Na2SO4ŗĶNaNO3µÄ»ģŗĻČÜŅŗ£¬Ń”ŌńŹŹµ±µÄŹŌ¼Į½«Ęä×Ŗ»ÆĪŖĻąÓ¦µÄ³Įµķ»ņ¹ĢĢ壬“Ó¶ųŹµĻÖCl-£¬SO42-ŗĶNO3-µÄĻą»„·ÖĄė£¬ŹµŃé¹ż³ĢČēĻĀ£ŗ
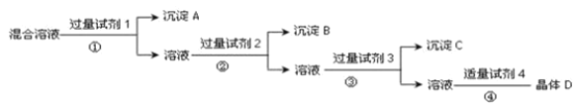
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öÉĻŹöŹµŃé¹ż³ĢÖŠĖłÓĆŹŌ¼ĮµÄĆū³Ę£ŗŹŌ¼Į1ĪŖ ___£¬ŹŌ¼Į2ĪŖ___£¬ŹŌ¼Į4ĪŖ_________”£
(2)¼ÓČė¹żĮæŹŌ¼Į3µÄÄæµÄŹĒ_________ ”£
(3)ŌŚ¼ÓČėŹŌ¼Į4ŗ󣬻ńµĆ¾§ĢåDµÄŹµŃé²Ł×÷¢ÜµÄĆū³ĘŹĒ_______”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com