
【题目】下列变化中,需加入氧化剂才能实现的是( )
A. Al(OH)3→Al2O3 B. FeCl3 →FeCl2 C. CuO→Cu D. Cl-→Cl2
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】下列不能用平衡移动原理解释的事实是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 氢气、碘蒸汽、碘化氢气组成的平衡体系加压后颜色变深
C. 淡黄绿色的氯水光照后颜色变浅
D. 合成氨工业反应过程中适时分离反应产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种新型清洁能源。回答问题:
(1)101KPa、25℃时,燃烧32g液态甲醇生成液态水和二氧化碳放热726.5kJ,则甲醇燃烧的热化学方程式为_____________
已知:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H=-24.5kJ·mol-1
CO(g)+2H2(g)![]() CH3OH(g) △H=akJ·mol-1
CH3OH(g) △H=akJ·mol-1
则2CO(g)+4H2(g)= CH3OCH3(g)+H2O(g) △H=__________
(2)工业上可用CO和H2制取甲醇,其热化学反应方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
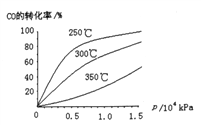
①△H______0(填“﹥”或“<”).判断依据是___________________
②为提高CO转化率,可采取的措施是_____________________________(至少答出两条)
③实际生产中,反应的条件控制在250℃,1.3×104kPa左右,选择此压强的理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂可用浓氨水来检验Cl2 是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)═6NH4Cl(固)+N2(气)
①用双线桥法标出电子转移的方向和数目
②若反应中消耗Cl21.5mol则被氧化的NH3在标准状况下的体积为 L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应NH3(g)+HCl(g)![]() NH4Cl(s)能自发进行,则该反应△H>0
NH4Cl(s)能自发进行,则该反应△H>0
B. 氨水溶液加水稀释后,溶液中 的值减小
的值减小
C. 1L1 molL-1的NaClO溶液中含有ClO-的数目为6.02×1023
D. 一定条件下,反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)>v逆(SO3)
2SO3(g)△H<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)>v逆(SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
A.常晒衣服、被子、床单等有利于身体健康
B.苯、CCl4均不溶于水,均易燃烧
C.乙烯能使溴水褪色,聚乙烯不能
D.煤通过干馏的方法可得到苯、甲苯、焦炭等物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能与Na反应放出H2,又能使溴水褪色,但不能使pH试纸变色的物质是( )
A. CH2===CH—COOH B. CH2===CH—CH2OH
C. CH2===CH—CHO D. CH2===CH—COOCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学常用的实验仪器: 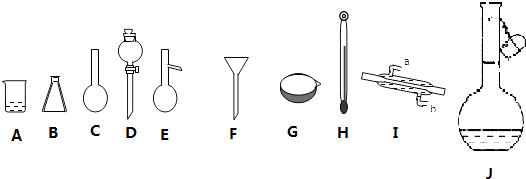
(1)填写以下仪器的名称:C , G .
(2)分离由乙醇和甘油组成的混合物需要用到的上述仪器有(填序号,下同)(已知乙醇和甘油互溶,沸点:乙醇78.5℃,甘油259℃);标有使用温度的仪器是 .
(3)填写除去下列混合物中的杂质需要的操作方法(括号内为杂质): NaCl溶液(泥沙); NaCl溶液(汽油);氯化钠固体(碘) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com