
 实验室用如图装置,利用Cu与HNO3反应来制取NO并用排水法收集气体.
实验室用如图装置,利用Cu与HNO3反应来制取NO并用排水法收集气体.分析 (1)铜与稀硝酸反应生成硝酸铜、一氧化氮和水;
(2)依据铜质量的减少量计算消耗的硝酸的物质的量,结合速率公式计算;铜与稀硝酸反应,消耗8mol硝酸,其中2mol表现氧化性,6mol表现酸性;
(3)图中采用排水法收集,收集的气体不能溶于水;
(4)加热、增大接触面积都能够加快反应速率;
(5)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,而生成NO2,再投入水中时发生反应:3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,据此解答.
解答 解:(1)铜与稀硝酸反应生成硝酸铜、一氧化氮和水,方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;
(2)消耗的铜的物质的量为$\frac{1.92g}{64g/mol}$=0.03mol,依据方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,可知消耗硝酸的物质的量为0.08mol,则5min内HNO3的反应速率=$\frac{0.08mol/0.02L}{5min}$=0.8mol/(L•min);铜与稀硝酸反应,消耗8mol硝酸,其中2mol表现氧化性,6mol表现酸性,消耗0.08mol硝酸,被还原的HNO3物质的量为0.02mol;
故答案为:0.8mol/(L•min);0.02mol;
(3)图中采用排水法收集,收集的气体不能溶于水,二氧化氮、氨气、二氧化硫都溶于水,不能用排水法收集,氮气不溶于水,可以用排水法收集;
故选:c;
(4)加热、增大接触面积都能够加快反应速率,稀释硝酸,氢离子浓度变小,反应速率减慢,使用浓硝酸反应生成二氧化氮,
故选:AB;
(5)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,而生成NO2,再投入水中时发生反应:3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,试管内气体又变为无色,
故答案为:试管内液面上升,气体恢复成无色.
点评 本题考查了一氧化氮的制备及有关方程式的计算,明确硝酸及氮的氧化物的性质及发生反应是解题关键,题目难度不大.


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:填空题

 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
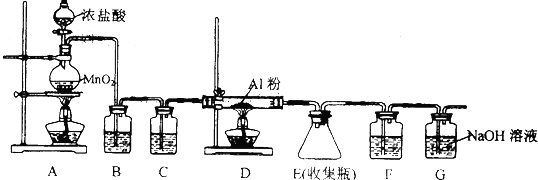
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入溴水,溴水褪色 | |
| B. | 将SO2气体通入滴入有酚酞的NaOH溶液中,红色褪色 | |
| C. | 将SO2通入品红溶液中,品红溶液褪色 | |
| D. | 将SO2通入酸性高锰酸钾溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 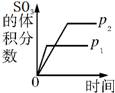 研究压强对反应的影响(p2>p1) | |
| B. |  研究温度对反应的影响 | |
| C. | 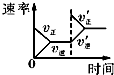 研究平衡体系中增加O2浓度对反应的影响 | |
| D. | 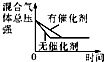 体积恒定的密闭容器中催化剂对反应的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 室温下,向20.00mL 1.000mol•L-1氨水中滴入1.000mol•L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法错误的是( )
室温下,向20.00mL 1.000mol•L-1氨水中滴入1.000mol•L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法错误的是( )| A. | a、d两点的溶液,水的离子积Kw(a)>Kw(d) | |
| B. | 将此氨水稀释,溶液的导电能力减弱 | |
| C. | c点时消耗盐酸体积V(HCl)<20 mL | |
| D. | 室温下,a点的氨水电离常数为$\frac{1{0}^{2(a-14)}}{1-1{0}^{a-14}}$ mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com