
用CH4催化还原NOx可以消除氮氧化合物的污染.例如:下列说法中错误的是( )
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ/mol.
A.等物质的量的CH4在反应①、②中转移电子数相同
B.由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l);△H>-574kJ/mol
C.4NO2(g)+2N2(g)=8NO(g);△H=+586kJ/mol
D.若用标准状况下4.48L CH4把NO2还原为N2,整个过程中转移的电子总数为1.6NA
科目:高中化学 来源:2015-2016学年云南省高二下学期期中化学试卷(解析版) 题型:选择题
相同质量的下列各烃,完全燃烧后生产CO2最多的是 ( )
A.甲烷 B.乙烷
C.乙烯 D.乙炔
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为:________________________。
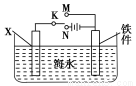
(2)利用右图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________处。
②若X为锌,开关K置于M处,该电化学防护法称为________。
(3)上图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量________3.2 g(填“<”“>”或“=”)。
(4)上图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是 ,若将开关K置于N处,发生的总反应是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:选择题
一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g)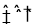 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
下列溶液中有关微粒的物质的量浓度关系正确的是( )
A.NaHRO3溶液中(R表示S和C):c(Na+)>c(HRO3-)>c(H+)>c(OH-)>c(RO32-)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③NH4HSO4三种溶液中水的电离程度:①>②>③
D.等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:N后>N前
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
一定温度下的可逆反应:A(g)+2B(g)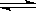 2C(g),下列叙述中能说明反应已达到平衡的是( )
2C(g),下列叙述中能说明反应已达到平衡的是( )
A.混合气体的物质的量不再变化
B.单位时间内消耗amolA,同时生成2amolC
C.容器内的压强不再变化
D.C生成的速率与C分解的速率相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期末化学试卷(解析版) 题型:填空题
氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
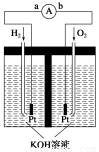
(1)负极反应式为________________________;正极反应式为__________________________。
(2)该电池工作时,H2和O2连续由外部供给,电池可连续不断地提供电能。因此,大量安全储氢是关键技术之一。
金属锂是一种重要的储氢材料,其吸氢和放氢原理如下:
Ⅰ.2Li+H22LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅱ中的氧化剂是________________;
②已知LiH固体密度为0.80g·cm-3,用锂吸收112 L(标准状况下)H2,生成的LiH体积与被吸收的H2体积比为__________(可用分数表示或用a×10-b表示,a保留两位小数);
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期末化学试卷(解析版) 题型:选择题
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )

A.电流从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为N2H4+4OH--4e-===N2↑+4H2O
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路一中高一下期末文科化学试卷(解析版) 题型:选择题
A、B、C、D、E是同周期的五种主族元素。A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A;C和D的最高价氧化物对应的水化物均呈酸性,且酸性C>D,E是这五种元素中原子半径最小的元素,它们的原子序数由小到大的顺序是( )。
A. A<B<C<D<E B. C<D<A<B<E C. B<A<D<C<E D. E<C<D<B<A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com