
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |


科目:高中化学 来源: 题型:
| A、酸碱中和滴定时,用10mL量筒量取10.00mL待测液 |
| B、用托盘天平称量25.20gNaCl固体 |
| C、常温条件下,用广泛pH试纸测得纯水的pH为7.0 |
| D、用500mL容量瓶配制480mL0.1000mol/LNaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25mL 3 mol?L-1的KCl |
| B、75 mL 1.5 mol?L-1的CaCl2 |
| C、150 mL 1 mol?L-1的NaCl |
| D、100 mL 2 mol?L-1的FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| P1 | P2 | P3 | |
| T1 | 0.10 | 0.04 | 0.02 |
| T2 | 0.20 | 0.16 | 0.05 |
| T3 | 0.40 | 0.35 | 0.20 |
| c(HCO3) | ||
c(C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 1 | 2 | 3 |
| 混合物质量/g | 4.36 | 5.54 | 9.81 |
| 硫酸溶液体积/mL | 50.00 | 50.00 | 50.00 |
| 生成SO2的物质的量/mol | 0.03 | 0.0375 | 0.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
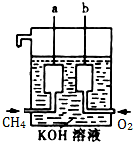 美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:
美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com