
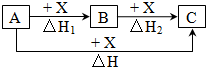
 一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )| A. | 只有②③④⑥ | B. | 除①外 | C. | 除⑤外 | D. | 全部 |
分析 由图可知,图示既是盖斯定律的应用,也是物质之间相互转化,符合转化关系的有变价物质的氧化反应、两性物质的转化以及多元酸对应的盐类之间的反应等,以此进行分析.
解答 解:①Fe$\stackrel{Cl_{2}}{→}$FeCl3,不存在上述转化,故不选;
②为C$\stackrel{O_{2}}{→}$CO$\stackrel{O_{2}}{→}$CO2,C$\stackrel{O_{2}}{→}$CO2的转化,符合,故选;
③为AlCl3$\stackrel{NaOH}{→}$Al(OH)3 $\stackrel{NaOH}{→}$NaAlO2的转化,AlCl3$\stackrel{NaOH}{→}$NaAlO2,符合,故选;
④为NaOH$\stackrel{CO_{2}}{→}$Na2CO3$\stackrel{CO_{2}}{→}$NaHCO3,NaOH$\stackrel{CO_{2}}{→}$NaHCO3,故选;
⑤S与氧气不能反应生成SO3,不符合A、X的转化,故不选;
⑥为Na2CO3$\stackrel{HCl}{→}$NaHCO3 $\stackrel{HCl}{→}$CO2的转化,Na2CO3$\stackrel{HCl}{→}$CO2,符合转化关系,故选;
故选A.
点评 本题考查考查常见元素及其化合物的有关转化,是中等难度的试题,对学生的要求比较高,学生需要有充足的知识储备,以及灵活应变能力,该题也可以通过排除法,进行筛选得到正确的答案.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液:K+、Cu2+、NO3-、AlO2- | |
| B. | 空气:CH4、CO2、SO2、NO | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br - | |
| D. | 各离子物质的量浓度相等的溶液:K+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,一氧化氮能与空气中的氧气直接化合 | |
| B. | SiO2与酸、碱均不反应 | |
| C. | Na2O、Na2O2组成元素相同,两化合物都为碱性氧化物 | |
| D. | NO2通入FeSO4溶液中始终无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaBr的电子式: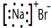 | B. | Na218O 中阴离子的结构示意图: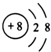 | ||
| C. | CH4的结构式: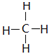 | D. | HF的电离方程式:HF?F-+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
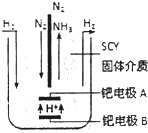 氨和联氨(N2H4)是氮的两种常见化合物,在工农业生产中有重要的应用.
氨和联氨(N2H4)是氮的两种常见化合物,在工农业生产中有重要的应用. [N2H5•H2O]++H+.下列盐酸肼溶液中的离子浓度关系正确的是ac(填序号).
[N2H5•H2O]++H+.下列盐酸肼溶液中的离子浓度关系正确的是ac(填序号).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com