
分析 反应中C元素化合价由0价升高到+4价,Cr元素从+6价降低到+3价,依据氧化还原反应得失电子守恒规律结合原子个数守恒规律书写方程式,氧化还原反应中所含元素化合价降低的反应物为氧化剂,对应还原产物,所含元素化合价升高的为还原剂,对应氧化产物.
解答 解:反应中C元素化合价由0价升高到+4价,Cr元素从+6价降低到+3价,所以K2Cr2O7作氧化剂,对应产物Cr2(SO4)3为还原产物,C做还原剂,对应产物CO2为氧化产物,要使氧化剂得到电子总数等于还原剂失去电子总数,则C系数为3,K2Cr2O7系数为2,依据原子个数守恒,反应方程式为:
3C+2K2Cr2O7+8H2SO4=3CO2+2K2SO4+2Cr2(SO4)3+8H2O;
故答案为:3;2; 8; 3; 2;2;8; K2Cr2O7;CO2;
点评 本题考查了氧化还原反应方程式配平及相关概念,明确氧化还原反应中各元素化合价变化及氧化还原反应得失电子守恒规律是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 实验 序号 | 温度℃ | 初始CCl4浓度 (mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳酸钠一过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
碳酸钠一过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5g | B. | 3g | C. | 6g | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
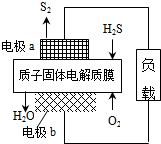 H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-=4 OH- | |
| C. | 电路中每流过4mol电子,电池内部释放632kJ热能 | |
| D. | 每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2-的离子半径大于Y+的离子半径 | |
| B. | H2Z的沸点高于H2X | |
| C. | Z的简单气态氢化物稳定性比W的强 | |
| D. | Y2X2和Y2Z的晶体类型和化学键类型完全相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com