
分析 (一)(1)根据n=$\frac{m}{M}$计算水、二氧化碳物质的量,进而确定n(C)、n(H),根据n=$\frac{V}{{V}_{m}}$计算氧气物质的量,根据O原子守恒计算有机物中含有O原子物质的量,据此解答;
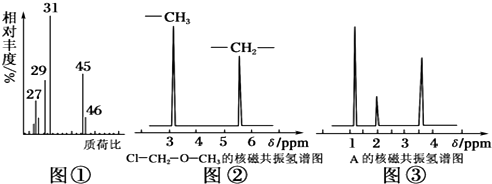
(2)根据质荷比可以确定相对分子质量,结合有机物分子中C、H、O原子数目之比确定分子式;
(3)结合A的分子式书写可能的结构简式;
(二)(4)有机物A的核磁共振氢谱中有3个吸收峰,说明有3种性质不同的H原子.
解答 解:(一)(1)5.4gH2O的物质的量=$\frac{5.4g}{18g/mol}$=0.3mol,则n(H)=0.6mol,8.8gCO2的物质的量=$\frac{8.8g}{44g/mol}$=0.2mol,则n(C)=0.2mol,
6.72LO2的物质的量$\frac{6.72L}{22.4L/mol}$=0.3mol,
由O元素守恒可知有机物中含有n(O)=0.3mol+0.2mol×2-0.3mol×2=0.1mol,
则n(C):n(H):n(O)=2:6:1,
所以有机化合物的实验式为C2H6O;
故答案为:C2H6O;
(2)有机化合物的实验式为C2H6O,由质荷比可知相对分子质量为46,则分子式为C2H6O,
故答案为:46;C2H6O;
(3)有机物A的可能结构简式有:CH3CH2OH、CH3OCH3,
故答案为:CH3CH2OH、CH3OCH3;
(二)(4)有机物A的核磁共振氢谱中有3个吸收峰,说明有3种性质不同的H原子,故A的结构为:CH3CH2OH,故答案为:3;CH3CH2OH.
点评 本题考查有机物结构确定,题目难度中等,从守恒角度判断有机物最简式为解答该题的关键,注意理解质谱图、核磁共振氢谱、红外光谱在有机物结构确定中的作用.


科目:高中化学 来源: 题型:选择题
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | Zn+2HCl═ZnCl2+H2↑ | ||
| C. | 2O3$\frac{\underline{\;催化剂\;}}{\;}$3 O2 | D. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
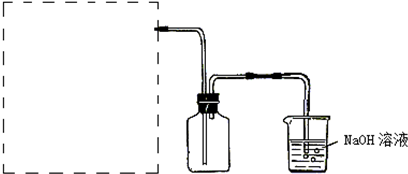
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ba2+、Ca2+、OH-、HCO3- | B. | H+、K+、NH4+、SO42- | ||
| C. | NO3-、SO42-、K+、Mg2+ | D. | H+、Na+、NO3-、Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
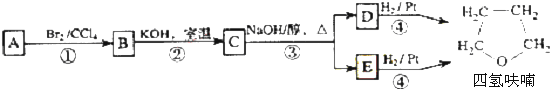
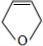 、
、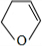 .
.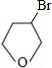 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$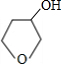 +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 点燃的镁条插入盛有二氧化碳的集气瓶里,则迅速熄灭 | |
| C. | 铝在高温下能还原锰、铁、铬等金属的氧化物 | |
| D. | 因为镁和铝在空气中都能形成氧化膜,所以镁和铝都不溶于浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AB | B. | BA2 | C. | AB4 | D. | B3A2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl原子所含质子数为18 | |
| B. | $\frac{1}{18}$mol的1H35Cl分子所含中子数约为6.02×1023 | |
| C. | 气体35Cl2的摩尔质量为70 | |
| D. | 3.5g的气体35Cl2的体积为2.24L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com