
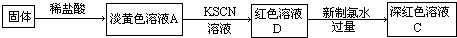
| 实验操作 | 预期现象 | 结论 |
| 取少量褪色后的溶液, | 说明假设一是合理的 |
| 实验操作 | 预期现象 | 只答对其中一方面均可得分 |
| 取少量褪色后的溶液,滴加20%KSCN溶液(2分) | 如果溶液变红色(2分) | |
| 或取少量褪色后溶液,加入0.1mol?L-1FeCl3溶液 | 或如果溶液不变红色 |


科目:高中化学 来源: 题型:
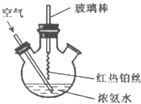
| A、反应后溶液中含有NO3- |
| B、反应后溶液中c(H+)增大 |
| C、实验过程中有化合反应发生 |
| D、实验过程中NH3?H2O的电离常数不可能发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
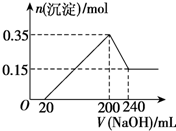 X、Y、R、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
X、Y、R、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| R | 在第3周期元素中,R的简单离子半径最小 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )
将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )| A、向硝酸银溶液中加入氯化钠固体,电流强度会减小 |
| B、向硝酸铜溶液中加入氢氧化钠固体,电流强度会减小 |
| C、将AgNO3溶液更换为Fe(NO3)3溶液,电流计指针偏转方向将相反 |
| D、当电流计指针为0时,该反应平衡常数K=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、②③④ |
| C、②③⑥ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
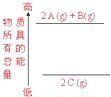 下列说法正确的是( )
下列说法正确的是( )| A、①③⑥ | B、②④⑤ |
| C、①③④ | D、③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com