
| A. | pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-) | |
| B. | pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-) | |
| C. | V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+) | |
| D. | V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>c(OH-)=c(H+) |
分析 A.pH>7时,c(H+)不可能大于c(OH-);
B.由溶液中的电荷守恒定律知:c(K+)+c(H+)=c(C6H5O-)+c(OH-),所以不可能满足c(K+)>c(C6H5O-)>c(H+)>c(OH-);
C.当加入苯酚的体积是20mL时,苯酚过量,溶液是由等物质的量浓度的苯酚和苯酚钾组成,所以根据物料守恒可知c(C6H5O-)+c(C6H5OH)=2c(K+);
D.苯酚是一种极弱的酸,所以当KOH溶液和苯酚恰好反应,产物苯酚钾会发生水解反应而显碱性.由题中数据可知,当二者恰好反应时消耗苯酚的体积是10mL,此时溶液中粒子的浓度大小关系为:c(K+)>c(C6H5O-)>c(OH-)>c(H+).
解答 解:A.溶液的pH>7时溶质可能为苯酚钠或苯酚钾与KOH的混合液,则溶液中一定存在c(OH-)>c(H+),故A错误;
B.溶液的pH<7时溶质为苯酚钾与苯酚的混合液,且苯酚的电离程度大于苯酚钾的水解,则c(H+)>c(OH-),再由电荷守恒c(K+)+c(H+)=c(C6H5O-)+c(OH-)可知c(C6H5O-)>c(K+),故B错误;
C.当苯酚溶液20mL,苯酚的物质的量恰好为钾离子物质的量的2倍,则由物料守恒可知c(C6H5O-)+c(C6H5OH)=2c(K+),故C正确;
D.当苯酚溶液10mL,二者恰好完全反应,溶液中的溶质为苯酚钾,由苯酚根离子的水解可知c(K+)>c(C6H5O-),故D错误;
故选C.
点评 本题考查溶液中离子浓度大小的比较,题目难度中等,明确反应后溶质组成为解答关键,然后根据水解反应原理、电荷守恒、物料守恒等知识即可解答.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2通入BaCl2溶液中无明显现象,说明碳酸的酸性比盐酸弱 | |
| B. | 氯水加入稀盐酸和AgNO3溶液产生白色沉淀,说明有氯水中有Cl-存在 | |
| C. | 常温下,Cu片投入到浓硫酸中不反应,因为浓硫酸使Cu产生钝化现象 | |
| D. | 浓硫酸具有脱水性,因而能使胆矾失去结晶水由蓝色变白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳的电子式: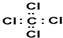 | B. | 氢氧根的电子式: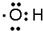 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的结构简式:CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性 F->Cl->Br- | B. | 碱性:Na(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性 HClO4>HBrO4>HIO4 | D. | 稳定性 HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
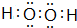 ,E的基态原子的外围电子排布式为3d24s2.
,E的基态原子的外围电子排布式为3d24s2.| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下80gSO2与33.6LCO2含氧原子数目均为3NA | |
| B. | 2molNO与1molO2混合后气体分子数小于2NA | |
| C. | 电解精炼铜时,阳极上粗铜质量减少6.4g,则电路中转化电子数为0.2NA | |
| D. | 1molCnH2n(烯烃)含有的共用电子对数为3nNA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
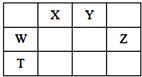 如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 物质WY2、W3X4均有熔点高、硬度大的特性 | |
| D. | T元素的单质不具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH与HCl的反应 | B. | 灼热的碳与二氧化碳的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl的反应 | D. | 酒精在空气中的燃烧反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com