
| A. | MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O | |
| B. | Ag+2HNO3(浓)→AgNO3+NO2↑+H2O | |
| C. | C+2H2SO4(浓)→CO2↑+2SO2↑+2H2O | |
| D. | 3Fe3O4+28HNO3(浓)→9Fe(NO3)3+NO↑+14H2O |
分析 根据酸中元素的化合价判断,化合价升高作还原剂,化合价降低作氧化剂,生成盐显酸性,据此分析.
解答 解:A.MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O,HCl作还原剂,部分生成氯化锰表现酸性,所以反应中酸起到了还原剂、酸的作用;
B.Ag+2HNO3(浓)→AgNO3+NO2↑+H2O,硝酸作氧化剂和酸;
C.C+2H2SO4(浓)→CO2↑+2SO2↑+2H2O,硫酸作氧化剂被还原为二氧化硫,硫酸只做氧化剂;
D.3Fe3O4+28HNO3(浓)→9Fe(NO3)3+NO↑+14H2O,硝酸作氧化剂和酸;
酸作还原剂的只有A,故A选;
故选A.
点评 本题考查了物质性质的分析应用,主要考查了硫酸、盐酸和硝酸在不同反应中的反应作用,元素化合价变化是分析的依据,题目较简单,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 可逆反应L(s )+aG(g)?bR(g)△H 达到平衡时、温度和压强对该反应的影响如图所示:x轴表示温度,y轴表示平衡混合气中G的体积分数,压强Pl>P2.下列判断正确的是( )
可逆反应L(s )+aG(g)?bR(g)△H 达到平衡时、温度和压强对该反应的影响如图所示:x轴表示温度,y轴表示平衡混合气中G的体积分数,压强Pl>P2.下列判断正确的是( )| A. | 1+a<b | |
| B. | △H<0 | |
| C. | a>b | |
| D. | 增加L的物质的量,可提高G的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
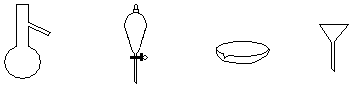
| A. | 蒸发、过滤、蒸馏、分液 | B. | 蒸馏、分液、蒸发、过滤 | ||
| C. | 蒸馏、过滤、蒸发、分液 | D. | 蒸发、分液、蒸馏、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
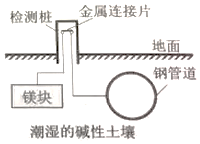
| A. | 该方法是将化学能转化成了电能 | |
| B. | 在此装置中钢管道做负极 | |
| C. | 该方法称为“外加电流阴极保护法” | |
| D. | 镁块上发生的电极反应:O2+2H2O+4e→4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,28 g CO 和 C2H4混合气体中的碳原子数为 NA | |
| B. | 1 mol N2 与 3 mol H2 充分反应,产物的分子数为 2NA | |
| C. | 标准状况下,11.2 L 己烷中含有的碳碳键数为 2.5NA | |
| D. | 32 g 硫粉与足量的 Cu 粉完全反应,转移的电子数为 2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
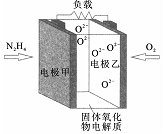 如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )
如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )| A. | 电池内的由O2-电极乙移向电极甲 | |
| B. | 电池的总反应为:N2H4+2O2═2NO+2H2O | |
| C. | 当甲电极上有1molN2H4消耗时,乙电极上有1molO2被氧化 | |
| D. | 电池外电路的电子由电极乙移向电极甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子排布为1s22s22p43s2的原子处于激发态 | |
| B. | 某元素质量数51,中子数28,其基态原子中未成对电子数为1 | |
| C. | 若某基态原子的外围电子排布为4d15s2,该元素原子核外有5个电子层 | |
| D. | BF3中B原子sp2杂化,为平面三角形 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com