
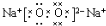
分析 A、B、C、D、E、F、G是原子序数依次增大的短周期元素,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,最高价氧化物对应水化物只有氢氧化铝能与酸、碱反应,故其中一种为氢氧化铝,另外为强酸与强碱,短周期内,强碱为氢氧化钠,原子序数E、F、G是原子序数依次增大,故E为Na元素,F为Al元素,G为S元素或Cl元素;A与B、C、D可分别形成10电子分子,A与E同主族,则A为H元素;D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,则D、G的原子序数中为2(1+11)=24,故D为O元素,G为S元素;B、C、D原子序数依次增大,都能与氢元素形成10电子分子,则B为碳元素,C为N元素,以此解答该题.
解答 解:A、B、C、D、E、F、G是原子序数依次增大的短周期元素,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,最高价氧化物对应水化物只有氢氧化铝能与酸、碱反应,故其中一种为氢氧化铝,另外为强酸与强碱,短周期内,强碱为氢氧化钠,原子序数E、F、G是原子序数依次增大,故E为Na元素,F为Al元素,G为S元素或Cl元素;A与B、C、D可分别形成10电子分子,A与E同主族,则A为H元素;D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,则D、G的原子序数中为2(1+11)=24,故D为O元素,G为S元素;B、C、D原子序数依次增大,都能与氢元素形成10电子分子,则B为碳元素,C为N元素.
(1)由上述分析可知,B为碳元素,处于周期表中第二周期第ⅣA族,
故答案为:第二周期第ⅣA族;
(2)上述元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是H2SO4,E、F元素最高价氧化物对应水化物分别为NaOH、Al(OH)3,二者反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:H2SO4;Al(OH)3+OH-=AlO2-+2H2O;
(3)Na在O2中燃烧生成化合物X为Na2O2,则X的电子式是: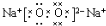 ,
,
故答案为: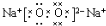 ;
;
(4)B单质与G的最高价含氧酸的浓溶液在加热条件下反应,为碳和浓硫酸的反应,方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
点评 本题考查结构性质位置关系应用,为高考常见题型,推断元素指关键,突破口为E、F、G元素最高价氧化物对应水化物之间可相互发生反应及A与B、C、D可分别形成10电子分子.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:推断题


 .
. 为有机原料制备化合物的合成路线流程图
为有机原料制备化合物的合成路线流程图 (无机试剂任选).合成路线流程图示例如下:
(无机试剂任选).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸碱中和反应是放热反应 | |
| B. | 要加热或高温才能进行的化学反应一定是吸热反应 | |
| C. | 物质发生化学反应一定要有新物质生成但不一定要伴随着能量变化 | |
| D. | 旧的化学键断裂会释放出能量,而要生成新化学键要吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色气体,难溶于水,密度比空气略小 | |
| B. | 乙烯燃烧时,火焰明亮,同时产生黑烟 | |
| C. | 与溴水发生取代反应而使溴水褪色 | |
| D. | 乙烯的产量标志着一个国家的石油化工水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 质子数相同的微粒,它们的化学性质基本相同 | |
| C. | 苯和溴苯的混合物可用分液法分离 | |
| D. | 由“C(石墨)→C(金刚石)△H=+1.9 kJ/mol”可知石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 1mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2与NaHCO3 | B. | SiO2与Na2CO3 | C. | SiO2 | D. | Na2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com