
【题目】利用太阳能分解水制氢,若光解0.02 mol水,下列说法正确的是
A.可生成H2的质量为0.02g
B.可生成氢的原子数为2.408×1023个
C.可生成H2的体积为0.224 L(标准情况)
D.生成H2的量理论上等于0.48 g Mg与足量稀盐酸反应产生H2的量
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物总共有5种物质:O2 、H2CrO4 、Cr(OH)3 、H2O、H2O2。已知该反应中H2O2 发生如下变化过程:H2O2 → O2 ,则有:
(1)该反应中的氧化产物_________________________;
(2)配平该反应的化学方程式并用单线桥表示电子转移情况:__________________________________________。
(3)现有反应:3BrF3 + 5H2O = HBrO3 + Br2 + 9HF + O2↑,已知BrF3中F的化合价为-1价,则有该反应中的氧化剂是____________,若生成0.5 mol Br2,则反应过程中转移电子为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
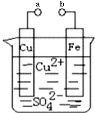
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为:Fe-2e-=Fe2+
C. a和b用导线连接时电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验操作中,正确的是( )
|
|
|
|
A.配制硫酸溶液时,将浓硫酸慢慢注入盛有水的容量瓶中进行配制 | B.用托盘天平称量药品时,将药品置于天平左盘 | C.将混合液蒸馏分离时,应使温度计水银球浸没在混合液中 | D.分液时,将上下层液体依次从分液漏斗下口分别流入两个烧杯中 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素①~⑩在周期表中的位置如下表所示:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)最外层电子数为2的元素有________(填元素符号);⑨的简单离子结构示意图为________,①与⑥以原子个数比为1:1形成的化合物的电子式为________,用电子式表示⑦与⑩形成化合物的过程________________________。
(
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈________色。⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为________。
(4)④、⑤、⑥的气态氢化物中最稳定的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
阴离子 | Cl- CO32— NO3— SO42— SiO32— I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是____________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是_____________________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有________;并据此推测原溶液应该呈_______________________________________________性,原因是_________________________________(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为__________________________________________________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含H+、SO42-、NO3-三种离子,其中H+、SO42-的物质的量浓度分别为7.0 mol·L-1和2.0 mol·L-1。取该溶液20 mL,加入3.2 g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
A. 0.75 LB. 0.336 LC. 1.5 LD. 0.448 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是分离混合物时常用的仪器,可以进行的混合物分离操作分别是()
![]()
A.蒸馏、过滤、萃取、蒸发B.蒸馏、蒸发、萃取、过滤
C.萃取、过滤、蒸馏、蒸发D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)铁原子外围电子轨道表示式为____________________,铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用_________摄取铁元素的原子光谱。
(2)FeCoOx是一种新型光电催化剂。第四电离能大小关系是I4(Co)____I4(Fe)(填“>”或“<” ) ,原因是_____________。
(3)二茂铁[(C5H5)2Fe]可用作火箭燃料添加剂、汽油抗爆剂。二茂铁熔点172℃,沸点249 ℃,易升华,难溶于水,易溶于有机溶剂,它属于_____________晶体。
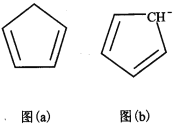
(4)环戊二烯(C5H6)结构如图(a),可用于制二茂铁。环戊二烯中碳原子的杂化方式为________。分子中的大π键可用符号![]() 表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H5―)结构如图(b),其中的大π键可以表示为_________________。
表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H5―)结构如图(b),其中的大π键可以表示为_________________。
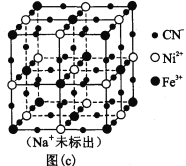
(5)某普鲁士蓝类配合物可作为新型钠离子电池电极材料。它由Na+、Ni2+、Fe3+和CN―构成,其晶胞结构如图(c)。该物质中,不存在________(填标号)。A.离子键 B. σ键 C. π键 D. 氢键 E. 金属键
(6)该晶胞中Fe3+采用的堆积方式与_______(选填Po、Na、Mg、Cu)相同,单个晶胞的配位空隙中共容纳_____个 Na+。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com