
【题目】把温度为20 ℃,浓度为1.0 mol/L的H2SO4溶液和2.2 mol/L的碱溶液各50 mL混合[溶液密度均为1g/mL,比热容为4.18 kJ/(kg·℃)]轻轻搅动,测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度t1 ℃ | 终止温度t2 ℃ |
H2SO4+NaOH | 20 | 33.6 |
H2SO4+NH3·H2O | 20 | 32.6 |
(1)反应NH3·H2O(aq)![]() NH4+ (aq)+OH-(aq)的焓变约____。
NH4+ (aq)+OH-(aq)的焓变约____。
(2)计算上述两组实验测出的中和热:ΔH1=___kJ/mol;ΔH2=__kJ/mol。
(3)由本题结论可预测将第1组中的1 mol/L的H2SO4溶液换成2mol/L的CH3COOH溶液进行实验,测得的中和热数值__(填“大于”“小于”或“等于”)56.848。
【答案】4.2kJ·mol-1 -56.848 -52.668 小于
【解析】
根据反应的焓变公式△H=-cm△T/n,
H2SO4与NaOH反应:①2H+(aq)+2OH-(aq)=2H2O(l)的焓变为-4.184×100×(33.620)/0.05×0.001kJ/mol=-113.8kJ/mol,
H2SO4与NH3H2O反应②2H++2NH3H2O(aq)=2NH4+(aq)+2H2O(l)的焓变为-4.184×100×(32.620)/0.05×0.001kJ/mol=-105.4kJ/mol
(1)②-①得到反应:NH3H2O(aq)![]() NH4+(aq)+OH-(aq)的焓变=(-105.4kJ/mol+113.8kJ/mol)×1/2=+4.2kJ/mol
NH4+(aq)+OH-(aq)的焓变=(-105.4kJ/mol+113.8kJ/mol)×1/2=+4.2kJ/mol
(2)根据分析,两个反应测定的中和热分别为ΔH1=-56.848kJ/mol;ΔH2=-52.668kJ/mol;
(3)醋酸溶液为弱酸,电离吸热,故测得的中和热数值小于56.848。


科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10L的密闭容器中充入1mol X和1mol Y进行反应:2X(g)+Y(g)![]() Z(g),60s后反应达到平衡,生成Z的物质的量为0.3mol。下列说法正确的是
Z(g),60s后反应达到平衡,生成Z的物质的量为0.3mol。下列说法正确的是
A.X的平衡转化率为40%
B.若将容器体积变为20L,则Z的平衡浓度小于原来的![]()
C.若增大压强,则Y的平衡转化率减小
D.若升高温度,X的体积分数增大,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:FeCl3+3KSCN![]() Fe(SCN)3+3KCl,离子方程式为:Fe3++3SCN-
Fe(SCN)3+3KCl,离子方程式为:Fe3++3SCN-![]() Fe(SCN)3,达到平衡后,进行下列操作,平衡怎样移动?
Fe(SCN)3,达到平衡后,进行下列操作,平衡怎样移动?
(1)加入少量FeCl3固体:平衡向____________移动;
(2)加入少量KSCN固体:平衡向____________移动;
(3)加入少量KCl固体:平衡____________移动,其理由是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.01mol·L-1MOH溶液的pH为10。已知:2MOH(aq)+H2SO4(aq)===M2SO4(aq)+2H2O(l) ΔH1=-24.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A. +33.1 kJ·mol-1 B. +45.2 kJ·mol-1
C. -81.5 kJ·mol-1 D. -33.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复合氧化钻![]() 可用于生产合金磁性材料、催化剂等。为充分利用资源,在实验室中探究采用含钴废渣(含
可用于生产合金磁性材料、催化剂等。为充分利用资源,在实验室中探究采用含钴废渣(含![]() 等)来制备复合氧化钴,具体流程如下:
等)来制备复合氧化钴,具体流程如下:

回答下列问题:
(1)![]() 的电子式为_______________________。
的电子式为_______________________。
(2)“碱煮水洗”的目的为______________________________________________。
(3)“酸浸”时,![]() 发生反应的离子方程式为_____________________________________________;滤渣1中主要成分的化学式为_______________________。
发生反应的离子方程式为_____________________________________________;滤渣1中主要成分的化学式为_______________________。
(4)检验“水洗液”中含有![]() 的操作和现象为______________________________________________。上述流程中多次应用过滤操作该操作所用主要玻璃仪器有_____________________。
的操作和现象为______________________________________________。上述流程中多次应用过滤操作该操作所用主要玻璃仪器有_____________________。
(5)下列装置中,适合进行“焙烧”操作的是_____________________(填选项字母)。
A. B.
B. C.
C. D.
D.
(6)称量![]() ,充分“焙烧”后得复合氧化钴
,充分“焙烧”后得复合氧化钴![]() ,则复合氧化钻的化学式为________________;“焙烧”过程中生成的气体能参与大气循环,则该过程_______________(填“有”或“无”)氧气参加反应。
,则复合氧化钻的化学式为________________;“焙烧”过程中生成的气体能参与大气循环,则该过程_______________(填“有”或“无”)氧气参加反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌空气燃料电池广泛用于铁路、航海灯标以及助听器中,其装置示意图如图所示。下列说法错误的是( )
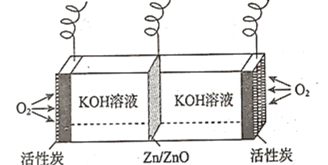
A.放电时,负极的电极反应式为![]()
B.放电时,![]() 向活性炭电极方向移动
向活性炭电极方向移动
C.充电时,![]() 电极上的电势比活性炭电极上的高
电极上的电势比活性炭电极上的高
D.充电时阴极质量减小![]() ,理论上阳极生成
,理论上阳极生成![]() 气体
气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 的捕捉和综合利用是目前研究的热点之一。回答下列问题:
的捕捉和综合利用是目前研究的热点之一。回答下列问题:
(1)科研工作者发现一种捕获二氧化碳生成甲酸的简单过程如图所示。
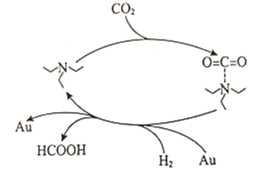
下列说法正确的是__________________(填选项字母)。
A.增大![]() 的物质的量可增大
的物质的量可增大![]() 的平衡产率
的平衡产率
B.![]() 和
和![]() 均能降低反应的活化能
均能降低反应的活化能
C.上述捕获过程能有效减少温室气体排放
(2)![]() 能用于制备二甲醚
能用于制备二甲醚
I.![]()
II.![]()
III.![]()
①二氧化碳气体与氢气生成二甲醚蒸气和水蒸气反应的热化学方程式为______________。
②![]() 时,在恒容密闭容器中发生反应I时,下列事实能说明该反应达到平衡状态的是_____________(填选项字母)。
时,在恒容密闭容器中发生反应I时,下列事实能说明该反应达到平衡状态的是_____________(填选项字母)。
A.气体的平均相对分子质量不再改变
B. ![]() 不再改变
不再改变
C.断裂![]() 键同时断裂
键同时断裂![]() 键
键
D.混合气体的密度不再改变
③![]() 时,向密闭容器中充入一定量
时,向密闭容器中充入一定量![]() ,发生反应Ⅱ,测得反应前压强为
,发生反应Ⅱ,测得反应前压强为![]() ,
,![]() 恰好达到平衡时,
恰好达到平衡时,![]() 的分压为
的分压为![]() ,则
,则![]() 内的反应速率
内的反应速率![]() _____________(用分压表示,下同);反应的平衡常数
_____________(用分压表示,下同);反应的平衡常数![]() _____________。
_____________。
④在催化剂条件下,发生反应![]() 。
。
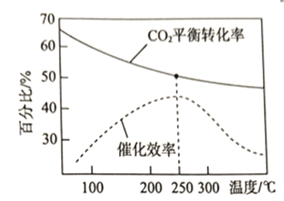
该反应的![]() ___________0(填“>”或“<”);
___________0(填“>”或“<”);![]() 的平衡转化率和催化剂的催化效率与温度的关系如图所示。则将反应温度选择为
的平衡转化率和催化剂的催化效率与温度的关系如图所示。则将反应温度选择为![]() 的原因为________________________________。
的原因为________________________________。
⑤向某绝热刚性容器中充入一定量的![]() 和
和![]() ,发生反应Ⅲ。容器内平衡压强______________________(填“大于”“小于”或“等于”)起始压强,原因为______________________。
,发生反应Ⅲ。容器内平衡压强______________________(填“大于”“小于”或“等于”)起始压强,原因为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学仿照“喷泉”实验的原理,在实验室中做了一个“喷烟”实验,如图所示。
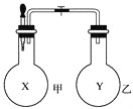
该同学在甲、乙两个烧瓶中分别充入X、Y两种无色气体,在胶头滴管中盛有含酚酞的氢氧化钠溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。若已知X、Y是氯化氢、氨气、氯气、氧气、甲烷、二氧化硫、一氧化氮七种气体中的两种,则下列判断中,正确的是( )
A. X是氨气,Y是氯化氢 B. X是氯气,Y是甲烷
C. X是二氧化硫,Y是氧气 D. X是一氧化氮,Y是氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科学、技术、社会、环境(STSE)密切联系。下列说法错误的是( )
A.新冠病毒可用75%乙醇、次氯酸钠溶液、过氧乙酸![]() 进行消毒,其消毒原理相同
进行消毒,其消毒原理相同
B.生产N95口罩的主要原料聚丙烯是一种高分子化合物
C.绿色化学要求从源头上消除或减少生产活动对环境的污染
D.聚乙烯是生产食品保鲜膜、塑料水杯等生活用品的主要材料,不能用聚氯乙烯替代
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com