
| A. | 过滤 | B. | 蒸发 | ||
| C. | 先过滤后蒸馏 | D. | 加入某种药品溶解浑浊的固体 |
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
| 混合物成分 | 提纯试剂 | 离子方程式 |
| ①FeCl2溶液(FeCl3) | ||
| ②FeCl3溶液(FeCl2) | ||
| ③Na2CO3溶液(NaHCO3) | ||
| ④Fe2O3(Al2O3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1L2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2NA | |
| B. | 7.8g苯中含有C=C键数目为0.3NA | |
| C. | 常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA | |
| D. | 用惰性电极电解1L浓度均为2mol•L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
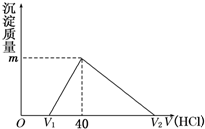 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )
将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )| A. | 图中m值为1.56 g | B. | 标准状况下产生氢气896 mL | ||
| C. | 图中V2为60 mL | D. | 原合金质量为0.92 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 s | B. | 30 s | C. | 5 s | D. | 1 s |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com