
| A£® | ”°±ł£¬Ė®ĪŖÖ®£¬¶ųŗ®ÓŚĖ®”±ĖµĆ÷ĻąĶ¬ÖŹĮæŗĶĪĀ¶ČµÄĖ®ŗĶ±ł£¬±łµÄÄÜĮæøß | |
| B£® | ”°Óń²»×Į²»³ÉĘ÷”±£¬”°°ŁĮ¶·½ÄܳÉøÖ”±·¢ÉśµÄ¾łĪŖ»Æѧ±ä»Æ | |
| C£® | ”°øŹÖ®ČēāĀ”±ĖµĆ÷ĢĒĄą¾łÓŠĢšĪ¶ | |
| D£® | ”°»šŹ÷Ņų»Ø”±ÖŠµÄŃ껚ŹµÖŹÉĻŹĒ½šŹōŌŖĖŲµÄŃęÉ«·“Ó¦ |
·ÖĪö A£®±ł×Ŗ»ÆĪŖĖ®µÄ¹ż³ĢĪüČČ£»
B£®”°Óń²»×Į²»³ÉĘ÷”±Ö»ŹĒÓńµÄŠĪדøı䣻
C£®µķ·ŪŗĶĻĖĪ¬ĖŲƻӊĢšĪ¶£»
D£®ŃęÉ«·“Ó¦ĪŖijŠ©½šŹōŌŖĖŲµÄŠŌÖŹ£®
½ā“š ½ā£ŗA£®±ł×Ŗ»ÆĪŖĖ®µÄ¹ż³ĢĪüČČ£¬Ņņ“ĖĻąĶ¬ÖŹĮæŗĶĪĀ¶ČµÄĖ®ŗĶ±ł£¬Ė®µÄÄÜĮæøߣ¬¹ŹA“ķĪó£»
B£®”°Óń²»×Į²»³ÉĘ÷”±Ö»ŹĒÓńµÄŠĪדøı䣬ŹĒĪļĄķ±ä»Æ£¬¹ŹB“ķĪó£»
C£®µķ·ŪŗĶĻĖĪ¬ĖŲŹōÓŚĢĒĄą£¬µ«Ć»ÓŠĢšĪ¶£¬¹ŹC“ķĪó£»
D£®ŃęÉ«·“Ó¦ĪŖŌŖĖŲµÄŠŌÖŹ£¬Ōņ½ŚČÕČ¼·ÅµÄŃ껚ŹĒijŠ©½šŹōŌŖĖŲŃęÉ«·“Ó¦Ėł³ŹĻÖ³öĄ“µÄÉ«²Ź£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ±ä»Æ”¢ŃęÉ«·“Ó¦µČÖŖŹ¶£¬Ę½Ź±±ŲŠė×¢ÖŲÖŖŹ¶µÄ»żĄŪ£¬²ÅÄÜÕżČ·½ā“š±¾ĄąĢāŠĶ£¬×¢ÖŲ»ÆѧÓėÉś»īµÄĮŖĻµ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£® £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | øƵē³ŲĶعżŃōĄė×ÓµÄŅĘ¶Æ£¬±£³ÖČÜŅŗÖŠµēŗÉĘ½ŗā | |
| B£® | µē³Ų¹¤×÷Ź±£¬µēĮ÷±ķÖøŹ¾³ö“ÓZn¼«µ½Cu¼«µÄµēĮ÷·½Ļņ | |
| C£® | µē³Ų¹¤×÷¹ż³ĢÖŠ£¬ŅŅ³ŲµÄc£ØSO42-£©Öš½„¼õŠ” | |
| D£® | µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬼׳ŲÖŠČÜŅŗÖŹĮæĆ÷ĻŌŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®| Ģ¼ĖįŃĪ | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| ČČ·Ö½āĪĀ¶Č/”ę | 402 | 900 | 1172 | 1360 |
| ŃōĄė×Ó°ė¾¶/pm | 66 | 99 | 112 | 135 |
 ŹĒ±ČC60Ō¼Ōē20ÄźŗĻ³É³öµÄŅ»ÖÖ¶Ō³ĘŠĶĢžĄą·Ö×Ó£¬¶ųĻÖČē½ńŅŃŗĻ³É³öŅ»ÖÖĮ¢·½ĶéÓėC60µÄø“ŗĻŠĶ·Ö×Ó¾§Ģ壬øĆ¾§ĢåµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬Į¢·½Ķé·Ö×ÓĢī³äŌŚŌC60¾§ĢåµÄ·Ö×Ó¼äæÕĻ¶ÖŠ£®ŌņøĆø“ŗĻŠĶ·Ö×Ó¾§ĢåµÄ×é³ÉÓƶžÕߵķÖ×ÓŹ½æɱķŹ¾ĪŖC8H8£®C60
ŹĒ±ČC60Ō¼Ōē20ÄźŗĻ³É³öµÄŅ»ÖÖ¶Ō³ĘŠĶĢžĄą·Ö×Ó£¬¶ųĻÖČē½ńŅŃŗĻ³É³öŅ»ÖÖĮ¢·½ĶéÓėC60µÄø“ŗĻŠĶ·Ö×Ó¾§Ģ壬øĆ¾§ĢåµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬Į¢·½Ķé·Ö×ÓĢī³äŌŚŌC60¾§ĢåµÄ·Ö×Ó¼äæÕĻ¶ÖŠ£®ŌņøĆø“ŗĻŠĶ·Ö×Ó¾§ĢåµÄ×é³ÉÓƶžÕߵķÖ×ÓŹ½æɱķŹ¾ĪŖC8H8£®C60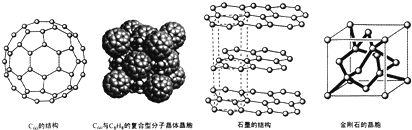
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ī“³ÉŹģĘ»¹ūµÄ¹ūČāÓöµāĖ®»į±äĄ¶ | |
| B£® | ÓėŠææéĻąĮ¬»ņÓėµēŌ“Õż¼«ĻąĮ¬£¬øÖĢśŅ»¶ØÄܱ»±£»¤ | |
| C£® | ĻĖĪ¬ĖŲŗĶÓĶÖ¬¾łæÉ·¢ÉśĖ®½ā£¬¶¼ŹōÓŚĢģČ»øß·Ö×Ó»ÆŗĻĪļ | |
| D£® | ¼ÓĆøĻ“ŅĀ·ŪæÉŅŌŗÜŗƵÄĻ“µÓĆ«ÖÆĘ·ÉĻµÄĪŪ×Õ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CµÄĢå»ż·ÖŹżŌö“ó | B£® | Ę½ŗāĻņÓŅŅĘ¶Æ | C£® | BµÄ×Ŗ»ÆĀŹĢįøß | D£® | a+b£¼c+d |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
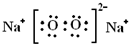 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com